
【题目】下列实验设计能达到实验目的的是
A.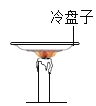 确定石蜡成分中含有碳元素
确定石蜡成分中含有碳元素
B.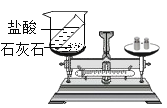 验证质量守恒定律
验证质量守恒定律
C. 探究燃烧的三个条件
探究燃烧的三个条件
D.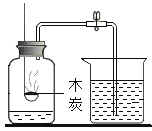 测定空气中氧气的体积分数
测定空气中氧气的体积分数
【答案】A
【解析】
A、根据实验的观察会发现冷盘子的底部变黑,则可确定石蜡中含有碳元素,符合题意;
B、因盐酸与碳酸钙反应生成二氧化碳气体,在烧杯中反应时二氧化碳气体逸出,则天平不会在反应前后保持平衡,达不到验证质量守恒定律的目的,不符合题意;
C、因在该实验中,白磷的着火点低,在实验中铜片上的白磷温度达到着火点,与氧气接触,能够燃烧,水中的白磷不与氧气接触,不能燃烧,该实验对比只能得出燃烧需要氧气,无法得出燃烧需要的所有条件,不符合题意;
D、因碳燃烧生成二氧化碳气体的体积与消耗氧气的体积相同,不好确定空气中减少的气体的体积,则不能达到测定空气中氧气的体积分数的目的,不符合题意。故选A。


科目:初中化学 来源: 题型:
【题目】酸、碱、盐在生产和生活中有广泛的应用。
(1)实验时同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是因为_____。
(2)粗盐中含有少量不溶性杂质(泥沙),还含有少量可溶性杂质(Na2SO4、CaCl2)。现以粗盐为原料制取精盐,除去杂质的操作为: I加水溶解: II 加过量BaCl2溶液; Ⅲ加过量的Na2CO3溶液; IV过滤: V加适量盐酸; VI蒸发结晶。请回答下列问题:
①实验操作步骤IV过滤和VI蒸发结晶都用到的玻璃仪器是_______。
②写出加过量BaCl2溶液时反应的化学方程式_________。
③加入过量Na2CO3溶液的目的是________。
(3)实验室配制一定质量分数的氯化钠溶液时,下列操作会导致溶液的质量分数偏小的是______(填序号)。
①用量筒量取水时仰视读数;
②将配好的溶液倒入试剂瓶中时有少量溅出;
③称量含不溶性杂质的氯化钠来配制溶液;
④所用砝码已生锈。
(4)氢氧化钠溶液与盐酸反应时溶液pH的变化如图所示。
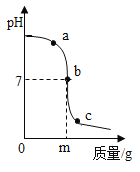
①下列说法正确的是______。
A c点所示溶液为碱性
B用酚酞溶液可以区分a、b、c三点处的溶液
C a点所示溶液中溶质为NaCl和NaOH
D该图所对应操作是将氢氧化钠溶液滴入盐酸中
②若改用mg硫酸与相同量氢氧化钠反应,所得溶液的pH___7(填“>” 、“<”或“=”)。
(5)某研究性学习小组对“氯碱工业”生产的烧碱样品中碳酸钠的质量分数进行如下探究:取10g烧碱样品加入到100g 稀盐酸中恰好完全反应,反应后测得溶液的质量为109.78g(气体的溶解忽略不记)。请计算该样品中碳酸钠的质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)为测定空气中氧气含量,某小组同学选用40mL的试管作反应容器和量程体积足够大且润滑很好的针筒注射器(如图) ,将足量白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹。用酒精灯加热白磷,燃烧结束后,待试管冷却后松开弹簧夹,观察现象。
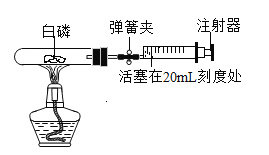
①开始实验前,该小组同学打开弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到活塞返回至20mL刻度处。该操作的主要目的是_______。
②实验后,可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约__处。
a 4mL刻度
b 8mL刻度
c 12mL刻度
d 16mL刻度
③下列实验操作,对实验结果有影响的是______。
a 装置漏气
b 白磷过量
c 燃烧结束后,立即松开弹簧夹,观察现象
(2)小婧同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体。但她在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体。
[提出问题]为什么会生成淡黄色固体?
[查阅资料]小婧查阅资料, 记录了下列几种物质的颜色:
物质 | MgO | MgCl2 | Mg3N2 | Mg( NO3)2 | Mg( OH)2 |
颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 |
[初步分析]其他同学认为不可能生成上表中的_____,理由是______。
[提出猜想]分析资料,小婧认为淡黄色固体可能是由镁与空气中的___反应生成的。
[实验探究]小婧设计实验证实了自己猜想。
[实验结论]根据小婧的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式:______;___。
[反思与评价]①空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释____。
②通过上述实验,你对燃烧有什么新的认识?_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一瓶久置的氢氧化钠溶液,为了探究该溶液是否变质以及变质的程度,设计了如下方案,根据方案流程,说法错误的是

A.由步骤①可知该氢氧化钠溶液已经变质
B.若步骤②中“现象I”生产白色沉淀,结论是该氢氧化钠溶液部分变质
C.若步骤②中“现象I”无明显现象,结论是该氢氧化钠溶液完全变质
D.步骤①中的CaCl2溶液可以用Ca(NO3)2溶液代替,也可以用Ca(OH)2溶液代替
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是以化合价为纵坐标,物质的类别为横坐标绘制的价类图。图中A-M是初中化学常见的九种物质(图中“→”表示一种物质转换成另一种物质),已知A和水反应放出大量的热,F中含有二种元素。
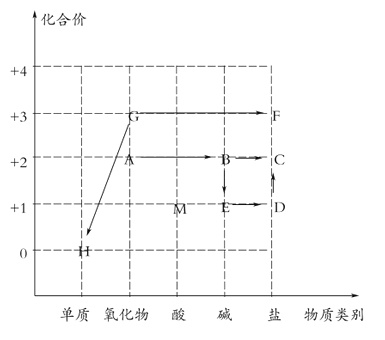
请回答下列问题:
(1)H的名称是______________。
(2)H、G均可与M溶液反应,分别生成含该金属元素的两种盐溶液。M与A反应的化学方程式为______________。
(3)D是由四种元素组成的化合物,向D溶液中加入一定量的B溶液,产生白色沉淀。过滤后取滤液,滴入过量M溶液,无明显现象,则滤液中的溶质是______________。(写出所有可能情况,填化学式)
(4)A-H八种物质中不能与M溶液反应的物质是______________。(填化学式)
(5)D→C反应的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室常用的实验装置:
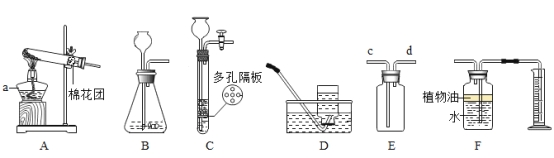
(1)写出下列仪器名称:a__________________。
(2)实验室用高锰酸钾制取氧气时,应选择的发生装置和收集装置是__ ( 填装置的字母代号) ,化学方程式是___,试管口放一团棉花的作用是____。
(3)若用E装置收集氢气,则氢气应从___口通入(填“c”或“d”)。
(4)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是__。
(5)装置C相对于装置B在操作方面的优势为____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸氢钠是小苏打的主要成分,在生产和生活中有许多重要的用途。化学课上,同学们为了解碳酸氢钠的性质,将一定质量的碳酸氢钠和稀硫酸混合,充分反应后,有气体逸出,写出该反应的化学方程式_____,同学们对反应后溶液中溶质的成分进行了探究:认为除一定含有硫酸钠外可能还含有其他成分,因此进行了猜想并做了如下实验:
(实验用品)pH试纸、锌片、氧化铜粉末、稀硫酸、氢氧化钠溶液、氯化钡溶液。
(猜想与假设)反应后溶液中溶质的可能组成成分。
猜想一:硫酸钠
猜想二:硫酸钠、碳酸氢钠
猜想三:硫酸钠、硫酸
(实验探究)同学们取反应后的溶液用不同方案进行如下实验,请根据结论完成如表实验现象中的空格。
实验方案 | A | B | C | D |
实验操作 |
|
|
|
|
实验现象 | _____ | 产生白色沉淀 | 试纸变色,对照标准比色卡,pH<7 | _____ |
实验结论 | 猜想二不正确 | 猜想三正确 | 猜想三正确 | 猜想三正确 |
(得出结论)猜想三正确。
(评价反思)
(1)老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在一处明显的操作错误是_____。
(2)有同学对实验方案B的结论提出了质疑,认为仅凭此现象不能得出猜想三正确,请说明理由_____。
(总结提高)依据所给实验用品,设计与上述实验不同的方案,确认猜想三是正确的,请你写出你的实验方案_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工厂欲测定铝土矿中Al2O3 的含量,将矿石粉碎(其中杂质既不溶于水也不与酸反应),进行如下实验:
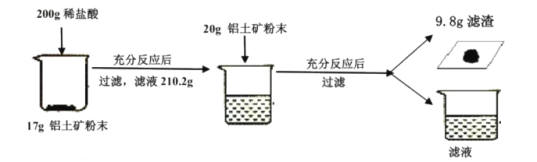
请回答下列问题:
(1)上述实验过程中发生反应的化学方程式为_____________。
(2)铝土矿中Al2O3的质量分数为_________________。
(3)根据已知条件列出求解200g稀盐酸中溶质质量(X)的比例式_________。
(4)若将最终所得溶液蒸发掉20. 4g水,所得不饱和溶液中溶质的质量分数为________。
(5)该炼铝厂每天用上述铝土矿170t来生产铝合金,则理论上日产含镁46%的铝镁合金的质量为_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据原子结构示意图和微观示意图填空:
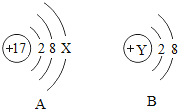
(1)如图A、B是两种微粒的微观示意图,请回答下列问题:
①若A是某元素的原子,则X=_____
②若B是某阳离子的结构示意图,则Y的数值可能是下列中的____(填字母)
A 11 B 10 C 9 D 8
③A、B属于不同元素的本质区别是____。
(2)在一定条件下,A、B能发生化学反应生成C和D,其微观示意图如下:
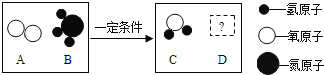
①若D为空气中体积分数最大的气体,则该反应中生成C和D的质量比为_____。
②若D为氮元素的+2价氧化物,则A、B的分子个数比为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com