
 (1)20℃时,甲物质的溶解度为______g;
(1)20℃时,甲物质的溶解度为______g;
(2)欲将40时℃乙物质的饱和溶液变为不饱和溶液,可采 用的方法是______;
(3)40℃时,将甲、乙两物质的饱和溶液各100g,分别降温到20℃,所得甲物质溶液的质量______(选填“>”或“=”或“<”)乙物质溶液的质量.
(4)下表为KCl在不同温度下的溶解度:
| 温度╱℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度╱g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 |
①由上表可推测KCl溶解度随温度的升高而______(填“增大”或“减小”).
②在10℃时,向100g水中加入40g KCl固体,充分混合溶解后所得溶液为______(填“饱和”或“不饱和”)溶液,此过程中的玻璃棒的作用为______;将其温度升高到50℃时,若不考虑溶剂的变化,则该溶液中溶质的质量分数为______(计算结果精确到0.1%).
解:(1)20℃时,甲物质的溶解度为40g;
(2)欲将40时℃乙物质的饱和溶液变为不饱和溶液,可采用的方法是加水或降温;
(3)40℃时,将甲、乙两物质的饱和溶液各100g,分别降温到20℃,由甲物质析出,故所得甲物质溶液的质量<乙物质溶液的质量.
(4)由表中KCl在不同温度下的溶解度可知:
| 温度╱℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度╱g | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | 51.1 |
①由上表可推测KCl溶解度随温度的升高而增大.
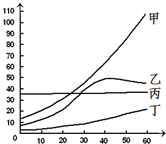
②在10℃时,因为其溶解度为31.0克,故可知向100g水中加入40gKCl固体,充分混合溶解后所得溶液为饱和溶液;此过程中的玻璃棒的作用为加快溶解速率;将其温度升高到50℃时,若不考虑溶剂的变化,则该溶液中溶质的质量分数为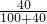 ×100%=28.6%.
×100%=28.6%.
故答为:
(1)40;
(2)加水或降温;
(3)<;
(4)①增大 ②饱和 加快溶解速率 28.6%


科目:初中化学 来源: 题型:阅读理解
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度(g) | 37.4 | 36 | 34.7 | 33.8 | 33.2 | X | 32.7 |
| 实验步骤 | 实验现象 | 实验结论 |
灼烧白色固体 灼烧白色固体 |
有特殊气味 有特殊气味 |
假设1成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 结合表列出几种物质在不同温度时的溶解度回答以下问题.
结合表列出几种物质在不同温度时的溶解度回答以下问题.| 温度/℃ | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | |
| 溶解度/g | 高锰酸钾 | 2.8 | 4.3 | 6.4 | 9.0 | 12.6 | 18.0 | 22.1 |
| 碳酸钠 | 7.0 | 12.5 | 21.5 | 39.5 | 49.0 | 48.0 | 45.0 | |
| 氯化钠 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | |
| 硝酸钾 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
查看答案和解析>>
科目:初中化学 来源:2013-2014学年河北省唐山市九年级12月月考化学试卷(解析版) 题型:填空题
下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
|
温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
|
溶解度/g |
Ca(OH)2 |
0.19 |
0.17 |
0.14 |
0.12 |
0.09 |
0.08 |
|
NaOH |
31 |
91 |
111 |
129 |
313 |
336 |
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是(填A或B)。

(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发
水后再恢复到原温度,⑥加入生石灰。其中措施正确的是 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 。
现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶
液中溶质的质量分数 乙 甲(填“>”、“<”或“=”)。
现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物 理方法是 。
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH
(填“偏大”、“偏小”或“不受影响”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
1)下图所示a、b、c、d四个点,表示可燃物容易着火的点是 点(填字母序号)。

(2)请根据下列反应的微观示意图分析:

参加反应的化合物A与化合物B的分子个数比为——,生成物中单质分子与化合
物分子的个数比为——。
(3)将一定质量的氯酸钾(不含催化剂)置于试管中加热一段时间,冷却后测得所得固体
中氯元素的质量分数为35.5%,则反应中已分解的氯酸钾的质量分数为——%。
(4)请根据下列图示回答问题:

①甲图中R物质在室温(20℃)时的饱和状态为D点,40℃时的饱和状态为A点,现将
甲图中的R溶液从A状态变到B状态,请设计并简述两个简单的实验操作途径:
a.——、 b.——; c.A状态由两种不同途径变到B状态时,溶液的溶质质量分数是否相等———(填“是” 或“否”)。
②乙图是表示M、N两种物质饱和溶液的溶质质量分数随温度变化的曲线。现分别向50g M、80g N固体中各加入150g水,并加热至完全溶解,同时各蒸发掉50g水,冷却至t℃,下列分析正确的是———(填序号,多选、少选、错选均不给分)。
a.只有N析出晶体; b.M、N两种溶液的溶质质量分数相等;
c.只有M析出晶体: d.M、N均有晶体析出:
e.M、N两种物质的溶解度相同。
查看答案和解析>>
科目:初中化学 来源:江西省模拟题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com