
| Ķ¬Ń§ | ČÜŅŗÖŠ¼ģŃé³öµÄĪļÖŹ |
| Š”Ć÷ | Na2SO4£¬Na2CO3 |
| Š”ŗģ | Na2SO4£¬BaCl2£¬Na2CO3 |
| Š”¾ü | Na2SO4£¬NaCl£¬Na2CO3 |
| A£® | ÓÉÓŚBaCl2ŗĶNa2SO4”¢Na2CO3¾ł²»¹²“ę£¬ĖłŅŌŠ”ŗģµÄ½įĀŪŅ»¶ØŹĒ²»ÕżČ·µÄ | |
| B£® | Š”Ć÷ŌŚČÜŅŗÖŠ¼ÓČėĮĖ×ćĮæµÄĻ”ĻõĖį£¬ĘäÄæµÄŹĒ¼ģŃéCO32-µÄ“ęŌŚ²¢½«Ęä³żČ„ | |
| C£® | Š”Ć÷½ÓĻĀĄ“ŌŚČÜŅŗÖŠ¼ÓČėĮĖ×ćĮæµÄBa£ØNO3£©2ČÜŅŗ£¬ÓĆĄ“¼ģŃéŹĒ·ń“ęŌŚSO42-£¬²¢½«²śÉśµÄ³ĮµķĶźČ«¹żĀĖ | |
| D£® | Š”¾üĶ¬Ń§ŌŚ±»²āČÜŅŗÖŠ¼ÓČėĮĖ×ćĮæµÄBaCl2ČÜŅŗ£¬¹żĀĖŗóŌŚĀĖŅŗÖŠ¼ÓČėĻõĖįŅųČÜŅŗŗó·¢ĻÖÓŠ°×É«³Įµķ£¬ĖµĆ÷ŌČÜŅŗÖŠŗ¬Cl-£¬ŌņŠ”Ć÷µÄ½įĀŪŅ²ŹĒ“ķĪóµÄ |
·ÖĪö øł¾Żø÷ÖÖĪļÖŹŌŚČÜŅŗÖŠÄÜ·ń¹²“ę¼°ŌŚ¼ģŃéĀČĄė×ÓŹ±£¬ĪŅĆĒæÉÓĆĻõĖįŅųŗĶĻ”ĻõĖį£»ŌŚ¼ģŃéĮņĖįøłĄė×ÓŹ±£¬ĪŅĆĒæÉÓĆĻõĖį±µŗĶĻ”ĻõĖį£»ĪŖĮĖÅųżĢ¼ĖįøłĄė×ÓµÄøÉČÅ£¬ĪŅĆĒæÉŅŌĻČ¼ÓĻõĖįÅųżĢ¼ĖįøłĄė×ÓµÄøÉČÅµČ½ųŠŠ·ÖĪö£®
½ā“š ½ā£ŗA”¢BaCl2ŗĶNa2SO4”¢Na2CO3Äܹ»·“Ó¦²śÉś³Įµķ£¬¾ł²»¹²“ę£¬Ņņ“ĖŠ”ŗģµÄ½įĀŪŅ»¶ØŹĒ²»ÕżČ·µÄ£¬¹ŹĖµ·ØÕżČ·£»
B”¢ĪŖĮĖČ·¶ØČÜŅŗÖŠŹĒ·ń“ęŌŚĮņĖįøłĄė×Ó”¢Ģ¼ĖįøłĄė×ÓŗĶĀČĄė×Ó£¬ŅŖČ·¶ØĀČĄė×ÓŗĶĮņĖįøłĄė×Ó£¬±ŲŠėÅųżĢ¼ĖįøłĄė×ÓµÄøÉČÅ£¬ĖłŅŌŹ×ĻČÓ¦¼ģŃé²¢³żČ„Ģ¼ĖįøłĄė×Ó£®ĖłŅŌæÉĻČ¼Ó¹żĮæµÄĻõĖį£¬¹Ū²ģŹĒ·ńÓŠĘųĢåÉś³É£¬¼ģŃé²¢³żČ„Ģ¼ĖįøłĄė×Ó£¬¹ŹĖµ·ØÕżČ·£»
C”¢ŅņĪŖĻõĖį±µŗĶĮņĖįøłĄė×Ó½įŗĻ²śÉśĮņĖį±µ³Įµķ£¬Ņņ“ĖŌŚČÜŅŗÖŠ¼ÓČėĮĖ×ćĮæµÄBa£ØNO3£©2ČÜŅŗ£¬ÓĆĄ“¼ģŃéŹĒ·ń“ęŌŚSO42-£¬¹ŹĖµ·ØÕżČ·£»
D”¢¼ÓČėĀČ»Æ±µ»įŅżČėĀČĄė×Ó£¬ŗĶĻõĖįŅų·“Ó¦²śÉś³Įµķ£¬Ņņ“Ė²»ÄÜČ·¶ØŌČÜŅŗÖŠŹĒ·ńŗ¬ÓŠĀČĄė×Ó£¬¹ŹĖµ·Ø“ķĪó£»
¹ŹŃ”ĻīĪŖ£ŗD£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖČÜŅŗÖŠµÄĄė×ӵļģŃéŗĶ¹²“ęĪŹĢā£¬ŌŚČ·¶ØČÜŅŗµÄ×é³ÉŹ±£¬Ź×ĻČŅŖ±£Ö¤ĖłČ·¶ØµÄČÜŅŗÖŠµÄČÜÖŹ±ŲŠė±£Ö¤ÄÜŌŚĶ¬Ņ»ČÜŅŗÖŠ¹²“ę£¬Ņ²¾ĶŹĒĖłČ·¶ØµÄČÜÖŹ²»ÄÜ·¢Éś»Æѧ·“Ó¦£¬×¢ŅāČÜÖŹÄÜŌŚĶ¬Ņ»ČÜŅŗÖŠ¹²“ęŹĒÖøČÜÖŹ²»ÄÜ·¢Éś»Æѧ·“Ó¦ŹĒ½ā“šµÄ¹Ų¼ü£®


 æĘѧŹµŃé»ī¶Æ²įĻµĮŠ“š°ø
æĘѧŹµŃé»ī¶Æ²įĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉÕ¼ī | B£® | ĻõĖįļ§ | C£® | ÅØĮņĖį | D£® | ĀČ»ÆÄĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH | B£® | MgCl2 | C£® | Na2CO3 | D£® | CaO |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
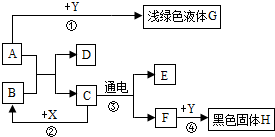 ČēĶ¼ĖłŹ¾£¬A”«HŹĒ³õÖŠ»Æѧ³£¼ūµÄĪļÖŹ£¬AŗĶBæÉ·¢ÉśÖŠŗĶ·“Ó¦£¬CĪŖÉś»īÖŠ×ī³£¼ūµÄŅŗĢ壬Fæɹ©øųŗōĪü£¬X³£ÓĆ×÷Ź³Ę·øÉŌļ¼Į£¬YĪŖµ„ÖŹ£¬Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ
ČēĶ¼ĖłŹ¾£¬A”«HŹĒ³õÖŠ»Æѧ³£¼ūµÄĪļÖŹ£¬AŗĶBæÉ·¢ÉśÖŠŗĶ·“Ó¦£¬CĪŖÉś»īÖŠ×ī³£¼ūµÄŅŗĢ壬Fæɹ©øųŗōĪü£¬X³£ÓĆ×÷Ź³Ę·øÉŌļ¼Į£¬YĪŖµ„ÖŹ£¬Ēėøł¾ŻĶ¼Ź¾»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com