
我国古代典籍中有“银针验毒”的记载,其反应原理之一是 4Ag+2H2S+O2=2X+2H2O。下列有关该反应的说法不正确的是
A. X 的化学式是 Ag2S B. H2S 中 S 元素为-2 价
C. 反应前后元素的种类不变 D. H2S 是无毒的
科目:初中化学 来源:广西壮族自治区北部湾经济区同城联考2019届九年级下学期中考一模化学试卷 题型:单选题
下面对有关实验的设计与解释,不合理的是()
选项 | 实验内容 | 试剂与方法 | 结论与解释 |
A | 分离CaCO3和CaO | 加水溶解、过滤 | CaO溶于水 |
B | 除去BaSO4中的BaCO3 | 加稀盐酸、过滤 | BaCO3溶于稀盐酸 |
C | 鉴别NaOH、Na2SO4溶液 | 滴加酚酞试液 | NaOH溶液显碱性 |
D | 检验溶液中的Mg2+ | 滴加NaOH | Mg(OH)2不溶于水 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源:天津市西青区2019届九年级第一学期期末考试化学试卷 题型:简答题
写出下列反应的化学方程式
(1)细铁丝在氧气中燃烧_____________________________;
(2)过氧化氢溶液中加入二氧化锰制氧气_________________________________________;
(3)一氧化碳燃烧___________________________________________;
(4)氢气还原氧化铜_________________________________________________。
查看答案和解析>>
科目:初中化学 来源:江苏省连云港市灌云县2019届九年级下学期期中考试化学试卷 题型:填空题
理化知识在生产、生活中有着广泛的应用。
(1)烧水时易产生水垢的水,属于_____水。
(2)我们每天应摄入一定量的_____来预防坏血病。
(3)保险丝(武德合金)比组成它的纯金属的熔点_____。
(4)用洗洁精除去油污,是由于洗洁精对油污有_____作用。
(5)尼龙手套、玻璃茶杯、纯棉桌布中,主要用有机合成材料制成的是_____。
查看答案和解析>>
科目:初中化学 来源:江苏省连云港市灌云县2019届九年级下学期期中考试化学试卷 题型:单选题
分类法是学习和研究物质的一种重要方法,下列分类正确的是( )
A. 生铁、黄金、金刚石﹣﹣合金
B. 纯碱、烧碱、熟石灰﹣﹣碱
C. 氮气、水银、氦气﹣﹣单质
D. 水、干冰、葡萄糖﹣﹣氧化物
查看答案和解析>>
科目:初中化学 来源:辽宁省葫芦岛市龙港区2019届九年级下学期中考一模化学试卷 题型:实验题
下列是初中化学中的一些常见实验,请回答下列问题:
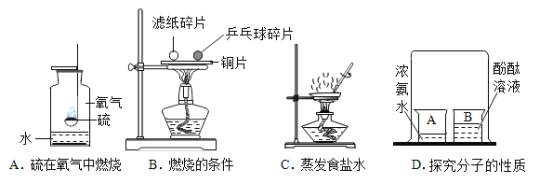
(1)A实验中,为了更好地吸收二氧化硫,可将水替换为_____溶液;(填一种具体物质名称)
(2)B实验中,可以说明燃烧的条件之一是_____;
(3)C实验中,玻璃棒不断搅拌的目的是_____;
(4)D实验中,一段时间后观察到的现象是_____。
查看答案和解析>>
科目:初中化学 来源:辽宁省葫芦岛市龙港区2019届九年级下学期中考一模化学试卷 题型:单选题
硼是作物生长必需的微量营养元素,硼元素的相关信息如图所示。下列有关硼的说法正确的是
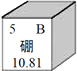
A. 相对原子质量为10.81g B. 属于金属元素
C. 原子的核电荷数为5 D. 原子核外有6个电子
查看答案和解析>>
科目:初中化学 来源:山东省青岛市李沧区2019届九年级下学期中考二模化学试卷 题型:综合题
海水中含有大量的氯化钠,工业上常用精制的氯化钠为原料制备纯碱,请你回答下列问题:
(1)从物质的元素组成上分析,需要加入含______元素的物质,但实际生产过程中,通常是先向饱和食盐水中通入氨气,制成饱和氨盐水,原因是______________________________________。
(2)工业上制得的纯碱中常含有少量的氯化钠(不考虑其它杂质),某化学兴趣小组的同学要测定某工厂生产的纯碱样品中碳酸钠的质量分数,设计如下方案:方案一:甲、乙、丙三位同学分別称取一定质量的样品放入烧杯中,溶入足量水后向滤液中加入一定质量的氯化钙溶液,充分反应后过滤,将沉淀洗涤、干燥并称量。相关实验数据记录如下表所示。
称量项目 | 甲 | 乙 | 丙 |
所取样品的质量/g | 12 | 12 | 15 |
加入氯化钙溶液的质量/g | 150 | 100 | 100 |
反应后所得沉淀的质量/g | 10 | 10 | 10 |
①请你分析上述数据,计算该样品中碳酸钠的质量分数。(写出计算步骤,计算结果保留到0.1%)______。
②方案二:丁同学用电子天平分别称取12g相同的碳酸钠样品和100g稀盐酸,充分反应后,测得烧杯内剩余物质的质量为108.6g,则该同学测得的碳酸钠的质量分数_________(填“大于”“小于”“等于”)方案一中测得的碳酸钠的质量分数。原因可能是_________________。(假设装置气密性良好)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com