
| A. | 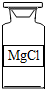 | B. | 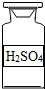 | C. | 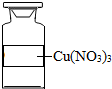 | D. |  |
分析 化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.
解答 解:A、氯化镁中镁元素显+2价,氯元素显-1价,其化学式为MgCl2,故选项化学式书写错误.
B、硫酸中氢元素显+1价,硫酸根显-2价,其化学式为H2SO4,故选项化学式书写正确.
C、硝酸铜中铜元素显+2价,硝酸根显-1价,其化学式为Cu(NO3)2,故选项化学式书写错误.
D、氧化铝中氧元素显-2价,铝元素显+3价,其化学式为Al2O3,故选项化学式书写错误.
故选B.
点评 本题难度不大,掌握化合物化学式的书写一般规律(金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零)是正确解答此类题的关键.


科目:初中化学 来源: 题型:选择题
| A. | 氯化铁溶液与氢氧化钠溶液反应后留下的红褐色固体 | |
| B. | 碱式碳酸铜受热分解后的黑色固体[Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑] | |
| C. | 用足量氢气还原氧化铜后留下的红色固体 | |
| D. | 盛放石灰水后留下的白色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
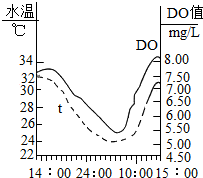 杭州市某郊区一条脏臭的小河,水体存在富营养化污染情况.右图水质监测站在2013年8月对此水体的一天DO(溶解氧)的实测数据,回答:(已知C-12 H-1 O-16 )
杭州市某郊区一条脏臭的小河,水体存在富营养化污染情况.右图水质监测站在2013年8月对此水体的一天DO(溶解氧)的实测数据,回答:(已知C-12 H-1 O-16 )| 水温/℃ | 25 | 26 | 27 | 29 | 31 | 32 | 34 |
| DO饱和值/mg•L-1 | 8.15 | 8.00 | 7.85 | 7.65 | 7.43 | 7.30 | 7.20 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
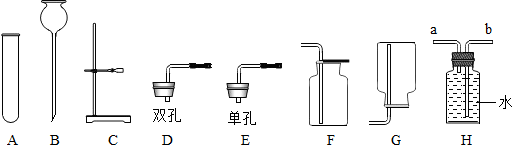
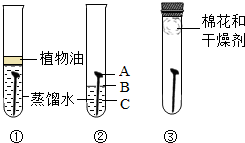 某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图所示:
某学习小组用相同的光亮铁钉探究生锈与哪些因素有关,设计的实验如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 食醋用于清除水壶中的水垢 | B. | 浓硫酸做某些气体的干燥剂 | ||
| C. | 二氧化碳作气体肥料 | D. | 用镁做军事照明弹 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 预期现象与结论 |
| 1 | 分别在A、B两只试管中各加入2mL反应后的混合溶液 | |
| 2 | 向A试管中滴加几滴品红溶液,再滴入足量的稀硫酸 | 有气泡产生,品红溶液褪色, 证明含有Na2SO3. |
| 3 | 向B试管中,加入足量的氯化钡溶液 | 再加入稀盐酸 ,证明含有Na2SO4,则猜想3成立. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com