
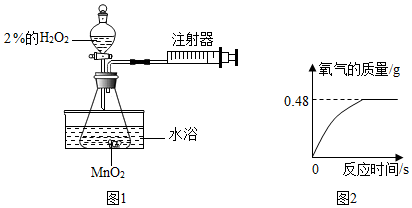
 ����Ϊ��̽���¶ȶ�H2O2�ֽ����ʵ�Ӱ�죬������ͼ��ʾװ�ã��г�װ����ȥ������ʵ�飨ˮԡ��������ˮ���м��ȣ���ʵ�����ݼ�¼�����ʾ��
����Ϊ��̽���¶ȶ�H2O2�ֽ����ʵ�Ӱ�죬������ͼ��ʾװ�ã��г�װ����ȥ������ʵ�飨ˮԡ��������ˮ���м��ȣ���ʵ�����ݼ�¼�����ʾ��| ʵ��1�� | ʵ��2�� | |
| MnO2������/�ˡ� | 0.5�� | 0.5�� |
| ��2%��H2O2�����/���� | 20�� | X�� |
| ���¶�/�� | 20�� | 80�� |
���� ��1�����ݶԱ�ʵ��̽���¶ȶ�H2O2�ֽⷴӦ����Ӱ��ķ���������
��2��������ͬ��ʱ���ڲ�������Ķ��ٷ�����
��3�������¶ȸ�ʱˮ������ˮ����������
��4����ͼʾ��֪����ȫ��Ӧ���������������Ϊ0.48g�����ݹ���������Һ�ֽ�Ļ�ѧ����ʽ������������������г�����ʽ�����ɼ�������뷴Ӧ��H2O2��������Ȼ���������������ʽ���㼴�ɣ�
��� �⣺��1�����öԱ�����̽���¶ȶ�H2O2�ֽⷴӦ���ʵ�Ӱ��ʱ������Ӧ���¶ȣ��������Ӧ��ͬ�����ԣ�ʵ��2��Ӧ����5%H2O240������
��2��������ʵ���У���ͨ����ͬ��ʱ����ע�����������������Ƚ�H2O2�ֽⷴӦ���ʵĴ�С��
��3��ʵ��2��ˮԡ�¶ȿ�����80��ʱ���ⶨ�ķ�Ӧ���ʻ����ʵֵƫ����ԭ�����ƿ���������������⣬�����¶Ƚϸ�ʱˮ������ˮ������
��4������ȫ��Ӧ����������������Ϊ0.48g�����ʵ���Ϊ$\frac{0.48g}{32g/mol}$=0.015mol
�ʴ�Ϊ��0.015mol��
������뷴Ӧ��H2O2������Ϊx��
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2��
68 32
x 0.48g
$\frac{68}{x}=\frac{32}{0.48g}$
��ã�x=1.02g
���뷴Ӧ�Ĺ�����������ʵ���Ϊ��$\frac{1.02g}{34g/mol}$=0.03mol��
�𣺸ù���������Һ�й�����������ʵ���Ϊ0.03mol��
����ƿ����������Һ����������$\frac{1.02g}{51g}��100%$=2%��
�ʴ�Ϊ����1��40����2����ͬ��ʱ����ע������������������3��ac����4��0.015��0.03mol��2%��
���� ������Ҫ����Ӱ�컯ѧ��Ӧ�ٶȵ����أ�ͬʱҲ�����˻����ķ����ᴿ���ۺ��ԱȽ�ǿ�����������п�����Ҫ����֮һ����Ҫ������ʵ�����У�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������Ӧ�÷dz��㷺�����������г��õĽ�����
������Ӧ�÷dz��㷺�����������г��õĽ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
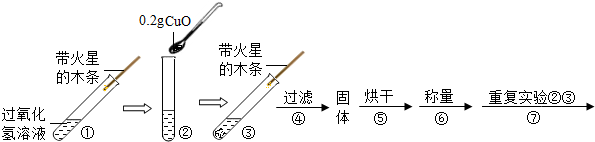
| ��������� | ������ | ��������� | ���� |
| ���������� | 0.2g | ���������� | �������� |
| �����������ݣ�������ľ����ȼ�� | ������0.2g | �����������ݣ�������ľ����ȼ | �������� |
| �����������ݣ�������ľ����ȼ | 0.2g | �����������ݣ�������ľ����ȼ | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | ����һƿ�����Ƿ�ΪCO2 | ��ȼ�ŵ�ľ������ƿ�� |
| B | ����H2��CH4 | �ֱ��ȼ���ڻ����Ϸ���һ�����ձ� |
| C | �����ٻƽ�ͭп�Ͻ� | ����� |
| D | �Ƚ�Zn��Cu��Ag�Ľ������ | ��Zn��Ag�ֱ����CuSO4��Һ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com