
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)碳酸钙高温分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(2)氧化铁与足量的稀盐酸反应生成氯化铁和水,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.
(3)CuO能与稀硫酸反应生成硫酸铜和水,铜不与稀硫酸反应,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:H2SO4+CuO═CuSO4+H2O.
(4)氧化钙与水反应生成氢氧化钙,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaO+H2O═Ca(OH)2.
(5)氧化钙与稀盐酸反应生成氯化钙和水,碳不与稀盐酸反应,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaO+2HCl=CaCl2+H2O.
(6)铁与稀硫酸反应生成硫酸亚铁溶液和氢气,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
(7)要除去NaOH溶液中的Na2CO3,实质就是除去碳酸根离子,可利用碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
故答案为:(1)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;(2)Fe2O3+6HCl═2FeCl3+3H2O;(3)H2SO4+CuO═CuSO4+H2O;(4)CaO+H2O═Ca(OH)2;(5)CaO+2HCl=CaCl2+H2O;(6)Fe+H2SO4═FeSO4+H2↑;(7)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 用石蕊试液鉴别H2O2和H2O | B. | 用澄清石灰水鉴别CO2和CO | ||
| C. | 用闻气味法鉴别酒精和白醋 | D. | 用点燃法鉴别棉纤维和羊毛 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该反应中涉及的物质都是氧化物 | |
| B. | 高铁酸钠中铁元素质量分数最大 | |
| C. | 化学计量数m=n | |
| D. | 该反应中,铁元素的化合价由+3价升高到+6价 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 托盘天平、烧杯、玻璃棒 | B. | 量筒、托盘天平、烧杯 | ||
| C. | 量筒、烧杯、玻璃棒 | D. | 量筒、玻璃棒 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 1 | 溶质 | 溶剂 |
| 氢氧化钠溶液 | 氢氧化钠 | 水 |
| 碘酒 | 碘 | 酒精 |
| 盐酸 | 氯化氢 | 水 |
| 石灰水 | 氢氧化钙 | 水 |
| 硫酸铜溶液 | 硫酸铜 | 水 |
| 白磷的二硫化碳溶液 | 白磷 | 二硫化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
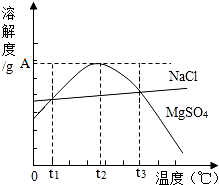 如图是NaCl、MgSO4的溶解度曲线.下列说法正确的是( )
如图是NaCl、MgSO4的溶解度曲线.下列说法正确的是( )| A. | 只有在t1℃时,NaCl和MgSO4的溶解度才相等 | |
| B. | t1℃~t2℃,MgSO4的溶解度随温度升高而增大 | |
| C. | 在t2℃时,MgSO4溶液的溶质质量分数最大 | |
| D. | 把MgSO4饱和溶液的温度从t3℃降至t2℃时,变成不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水、硝酸银、稀硝酸 | B. | 水、氢氧化钠、稀盐酸 | ||
| C. | 水、氢氧化钾、稀硝酸 | D. | 水、氢氧化钾、稀盐酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com