
| A. | 金属或合金 | B. | 氧化物 | C. | 有机物 | D. | 盐 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
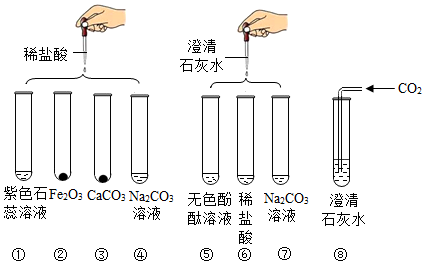
| 步骤 | 操作 | 现象 | 结论 |
| 第一步 | 取样,加入少量盐酸 | 无气泡产生 | 废液中一定没有碳酸钠 |
| 第二步 | 再次取样,进行实验⑧ | 无白色沉淀产生 | 废液中只有氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 洗气瓶乙中浓硫酸的作用是干燥氢气 | |
| B. | 丙装置中的氧化铜没有完全被还原,会影响实验结果 | |
| C. | 实验中,通过测定丙、丁装置质量的改变值,就能达到测定水的组成的目的 | |
| D. | 该装置存在缺陷,应该在丁装置后再连接一个盛碱石灰的干燥管 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
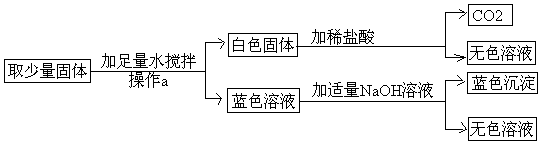
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用小苏打治疗胃酸过多 NaCO3+2HCl═2NaCl+H2O+CO2↑ | |
| B. | 实验室用过氧化氢溶液制取氧气 2H2O2═2H2O+O2↑ | |
| C. | 用石灰水检验二氧化碳 Ca(OH)2+CO2=CaCO3+H2O | |
| D. | 用盐酸除去铁锈 Fe2O3+6HCl=2FeCl3+3H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
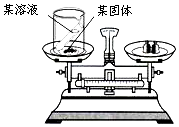 某科学兴趣小组的同学利用如图所示实验装置验证化学变化中的质量守恒.下列各种药品组合中,他们应选用( )
某科学兴趣小组的同学利用如图所示实验装置验证化学变化中的质量守恒.下列各种药品组合中,他们应选用( )| A. | 氯化钠固体和水 | B. | 稀硫酸和镁粉 | ||
| C. | 稀盐酸和银粉 | D. | 氯化钙溶液和碳酸钠粉末 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
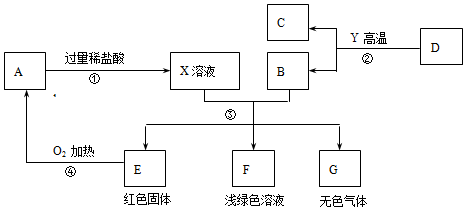
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
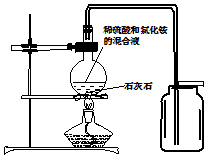 实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,原因是生成的硫酸钙是一种微溶物,会覆盖在石灰石的表面,阻止反应的进一步进行.某小组经过研究,用如图所示方法成功制得了大量CO2(反应物为稀硫酸和石灰石).
实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,原因是生成的硫酸钙是一种微溶物,会覆盖在石灰石的表面,阻止反应的进一步进行.某小组经过研究,用如图所示方法成功制得了大量CO2(反应物为稀硫酸和石灰石).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com