
| A. |  滴加药品 | B. | 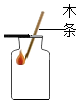 氧气验满 | C. |  液体加热 | D. | 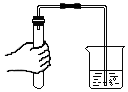 气密性检查 |
分析 A、根据胶头滴管的使用方法进行分析判断;
B、根据氧气验满的方法进行分析判断;
C、根据给试管中的液体加热的方法进行分析判断;
D、根据检查装置气密性的方法进行分析判断.
解答 解:A、使用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误;
B、氧气验满时,应将带火星的木条放在集气瓶口,不能伸入瓶中,图中所示操作错误;
C、给液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能超过试管容积的$\frac{1}{3}$,大拇指要握在试管夹的长柄处,图中所示操作错误;
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气,图中所示操作正确.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | A | B | C | D |
| 实验设计 | 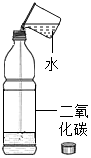 | 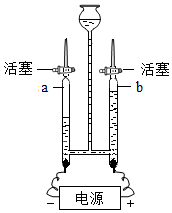 | 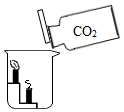 | 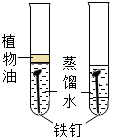 |
| 实验目的 | 证明二氧化碳与水反应生成碳酸 | 证明水是由氢元素和氧元素组成的 | 只能证明二氧化碳的密度比空气大 | 证明铁生锈是水和氧气共同作用的结果 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 鸡蛋壳的质量 | 空烧杯的质量 | 充分反应后,烧杯及内容物的总重量 |
| 16g | 60g | 155.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
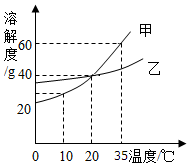
| A. | 10℃时,甲的溶解度小于乙的溶解度 | |
| B. | 甲的溶解度大于乙的溶解度 | |
| C. | 20℃时,把30g甲放入50g水中形成的溶液中溶质与溶剂的质量比为3:5 | |
| D. | 等质量的甲、乙饱和溶液,从35℃降温至10℃时,二者溶质质量分数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com