
【题目】煤、石油和天然气是重要的、不可再生的能源,它们燃烧产生过多的二氧化碳等物质会对环境造成严重的影响。我国政府高度重视“节能减排”,确定我国今年“世界环境日”的主题和标识。
(1)下列措施符合我国“世界环境日”主题的是____________。(填字母)
A.限制发展高耗能的产业
B.推广使用“乙醇汽油”,减少有害气体排放
C.为了减少废气对本地区空气的污染, 化工厂加高烟囱
D.将污染严重的工厂迁到农村去
(2)天然气的主要成分是_______(填名称),其完全燃烧的化学方程式为_____________。
(3)图2中的信息告诫人类:二氧化碳等气体过多的排放,使_______________加剧,导致全球变暖。为减少二氧化碳过多的排放对环境的影响,你能做的一件事____________________;科学家采取“组分转化”技术,将二氧化碳和氢气以一定比例混和,在一定条件下反应,生成一种重要的化工原料乙烯(C2H4)和水。该反应的化学方程式为_____________________________。
(4)为解决能源短缺和环境污染的问题,目前有待开发、利用的新能源有_______________。(写一种)
(5)“绿箱子环保计划——废弃手机及配件回收联合行动”已在全国许多重点城市中相继开展,废弃手机中的金属材料回收利用的意义,你认为有_______________(举出一个方面)。
【答案】 A 、B 甲烷(CH4) CH4 + 2O2 ![]() CO2 + 2H2O 温室效应 植树造林(合理答案均可) 2CO2+6H2
CO2 + 2H2O 温室效应 植树造林(合理答案均可) 2CO2+6H2![]() C2H4 +4H2O 氢能(合理答案均可) 可以节约金属资源;可以节约冶炼相关金属所消耗的能源;可以减少对环境的污染。(任写一点)
C2H4 +4H2O 氢能(合理答案均可) 可以节约金属资源;可以节约冶炼相关金属所消耗的能源;可以减少对环境的污染。(任写一点)
【解析】(1)限制发展高耗能的产业、推广使用“乙醇汽油”符合我国“世界环境日”主题,故答案为AB;
(2)天然气的主要成分是甲烷;甲烷燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2![]() CO2+2H2O;
CO2+2H2O;
(3)二氧化碳是一种重要的温室气体,植树造林可以减缓温室效应;二氧化碳和氢气反应生成乙烯和水的化学方程式为:2CO2+6H2![]() C2H4+4H2O;
C2H4+4H2O;
(4)目前有待开发、利用的新能源有太阳能、氢能、风能、水能、地热能等能源;(5)废弃手机中的金属材料回收,可以再次进行利用,可以节约金属资源;手机中的一些重金属废弃后会污染土壤、水资源等,回收后可以减少对环境的污染;减小了由于冶炼金属而消耗的能源等(合理即可)。


科目:初中化学 来源: 题型:
【题目】小明同学依据描述书写的化学符号:①两个氮分子:2N2;②由三个氧原子构成的臭氧分子:3O;③粒子结构示意图 表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+。其中,正确的是( )
表示的粒子:S;④两个铁离子:2Fe3+;⑤导电、导热性最好的金属:Ag;⑥+2价的镁元素:Mg2+。其中,正确的是( )
A.②④⑤ B.①④⑤ C.①③⑤ D.①④⑥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能在pH=11的溶液中大量共存,且溶液为无色透明的一组物质是 ( )
A. AlCl3、CuSO4、NaCl B. BaCl2、NaCl、NaOH
C. CaCl2、Na2CO3、AgNO3 D. K2SO4、NaNO3、NH4Cl
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】汽车是现代生活中不可缺少的代步工具。请回答下列问题:
(1)下列汽车配件及用品中,属于有机合成材料的是(填序号)_____。

a.钢铁外壳 b. 合成纤维材质的安全气囊 c.橡胶轮胎 d.羊毛座垫
(2)铁易锈蚀,铁生锈的条件是________。喷漆前需将铁制品放入稀盐酸中除锈(铁锈主要成分是Fe2O3),观察到溶液变黄,有无色气泡逸出。溶液变黄的化学方程式为_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】酸、碱、盐是工业和生活中应用比较广泛的化学物。用你一年来所学的有关酸碱盐的知识回答下列问题:
(1)下列物质存放在烧杯中,一段时间后,质量变大且变质的是__________。
①浓盐酸 ②浓硫酸 ③烧碱 ④澄清石灰水 ⑤食盐
(2)把50g质量分数为98℅的浓硫酸稀释为20℅的硫酸用于下面的实验,需要水的质量是______。
(3)某化学兴趣小组的同学问一定量NaHCO3的溶液中加入一定量的稀H2SO4。待反应量是完全后(假设反应所产生的气体全部逸出),对反应后溶液中的溶质的成分进行如下探究:
[实验用品]pH试纸、Zn片、氧化铜粉末、稀H2SO4、NaOH溶液、BaC2l溶液.
[假设猜想]猜想一:Na2SO4;猜想二:Na2SO4、NaHCO3;猜想三:Na2SO4、H2SO4。
[实验探究]同学们取反应的溶液用不同方案进行如下实验,请根据现象或结论填空。
实验方案 | A | B | C | D |
操作 |
|
|
|
|
现象 | 无气泡产生 | 试纸变色,对照比色卡,pH<7 | ① _______ | 产生白色沉淀 |
结论 | ②______ | 猜想三正确 | 猜想三正确 | 猜想三正确 |
[得出结论]猜想三正确
[评价反思]老师对同学们能用多种方案进行探究,并且得出正确的实验结论给予了肯定,同时指出探究中存在的两处明显错误,分别是:
③__________;④_________。
[总结提高]依据所级实验用品,你还有什么不同的方法确认猜想三是正确的,请写出你的实验方案。
⑤____________。
(4)胃酸过多的病人,通常需每天服用含碳酸钠的药物9片,能消耗胃酸中的氯化氢2.19g。某病人有胃溃疡病症,这种药物会加剧胃部疼痛,医生建议改用含氢氧化铝(其他成分不与胃酸反应)的胃舒平,药物标签如图所示。请计算中和相同质量的胃酸,每天需要服用胃舒平多少片?____________

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将49g氯酸钾与4g二氧化锰的混合物加热到质量不再减少为止,得剩余固体为33.8g,则反应生成氧气的质量为________g,同时生成________g氯化钾.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献,工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质,现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。
试求:(1)该纯碱样品的纯度(计算结果精确到0.1%)
(2)所得溶液中溶质的质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】聚合硫酸铁(PFS)是一种新型的饮用水处理剂和城市污水净化剂,其化学组成可表示为[Fex(OH)y(SO4)z]m。某中学化学兴趣小组以聚合硫酸铁的生产流程和相关性质进行了一系列的探究。
Ⅰ.聚合硫酸铁的工业生产。
如图是以回收废铁屑为原料制备PFS的一种工艺流程。
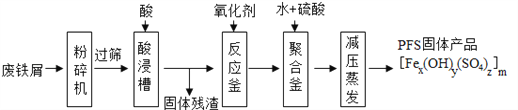
回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为______。“过筛”与化学实验中的______原理相似(填操作名称)。
(2)酸浸时最合适的酸是______,写出铁锈与该酸反应的化学反应方程式______。
(3)反应釜中加入氧化剂的作用是将Fe2+转化为Fe3+。你认为下列氧化剂中最合适的是
______(填标号),原因是______。
A.KMnO4 B.Cl2 C.H2O2 D.HNO3
(4)相对于常压蒸发,减压蒸发的优点是______。
A.有利于水分蒸发 B.降低沸点,防止晶体分解 C.降低生产成本
Ⅱ.聚合硫酸铁的成分探究。
该研究小组为确定聚合硫酸铁的化学式,进行了如下实验:
①称取5.52 g聚合硫酸铁样品溶于足量的稀盐酸中并充分混合;
②向①所得的混合物中加入足量的BaCl2溶液,充分反应后,经过滤、洗涤、干燥、称重,得沉淀4.66 g。
③若向步骤②的滤液中加入过量的NaOH溶液,充分反应后,再将沉淀过滤、洗涤、灼烧、称重,得固体3.20 g。
则聚合硫酸铁[Fex(OH)y(SO4)z]m样品中的x:y:z的值为______。
试写出该聚合硫酸铁与盐酸的反应方程式______。
Ⅲ.聚合硫酸铁的热分解气体产物成分探究。
该小组将5.52 g聚合硫酸铁在一定条件下加热完全分解,对所得气体产物进行实验探究。(已知SO3的熔点为16.8℃)。
【提出假设】
假设1:所得气体的成分是SO3;
假设2:所得气体的成分是SO2、O2;
假设3:所得气体的成分是______。
【设计实验】
按下图装置进行实验。
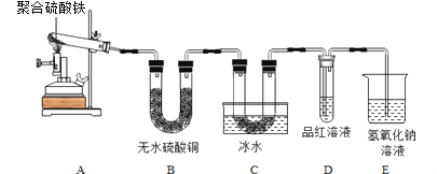
实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是______。
【实验结论】
通过实验现象判断,假设______成立。
如果最终试管中固体为一种红棕色纯净物,则质量为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列各组物质的俗称、化学式、用途不一致的是
A. 生石灰—CaO —做干燥剂 B. 纯碱—NaOH —治疗胃酸过多
C. 小苏打— NaHCO3—发酵粉 D. 干冰—CO2—人工降雨
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com