
【题目】某兴趣小组同学阅读课外资料得知:很多因素都能影响过氧化氢分解速度。于是同学们探究影响过氧化氢分解速度的某种因素。
【实验过程】实验数据记录如下:
过氧化氢溶液的质量 | 过氧化氢溶液的浓度 | MnO2的质量 | 测量数据 | |
Ⅰ | 50.0g | 1% | 0.1g | 9 mL |
Ⅱ | 50.0g | 2% | 0.1g | 16 mL |
Ⅲ | 50.0g | 4% | 0.1g | 31 mL |
【实验分析】
(1)过氧化氢分解的化学方程式为______________________________________。
(2)表格中的“测量数据”的指的是:相同时间内_________________________________。
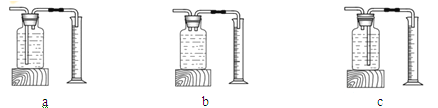
(3)本实验中,测量O2体积的装置是________(填编号)。
【实验结论】
在相同条件下______________________________________________。
【交流评价】
(1)甲同学提出在上述实验中测量______________同样能得出相同的结论。
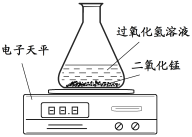
(2)乙同学提出用下图装置进行实验,通过比较____________________也能达到实验目的。
【实验反思】
除了上述因素会影响过氧化氢分解速度外,___________(写一种)也会影响过氧化氢分解速度,你的实验方案是__________________________________________________________________。
【答案】【实验分析】(1)2H2O2 MnO2 2H2O + O2↑
(2)相同时间内收集氧气的体积
(3)C
【实验结论】双氧水浓度越大,产生氧气速度越快
【交流评价】
(1)收集等体积氧气所需要的时间
(2)电子天平的读数不再发生变化时,所需要的时间
【实验反思】
催化剂的种类(温度等)
分别取等质量等浓度的过氧化氢溶液,依次加入等量、不同种类的催化剂,记录收集等体积氧气所需要的时间
【解析】
试题分析:过氧化氢分解生成水和氧气:2H2O2 MnO2 2H2O + O2↑;探究影响过氧化氢分解速度的某种因素要通过比较相同时间内收集氧气的体积,收集到的氧气的量越大,说明反应速率越快;测量O2体积可通过测量排出的水的体积来判断,故选C装置;通过该实验可以发现双氧水浓度越大,产生氧气速度越快;探究影响过氧化氢分解速度的某种因素要通过比较相同时间内收集氧气的体积,或收集相同体积的氧气所需时间的长短;过氧化氢分解产生的氧气会逸散到空气中,该装置可通过电子天平的读数不再发生变化时,所需要的时间,时间越短,说明反应速率越快;温度和催化剂也会影响过氧化氢的分解速率,但要采用控制变量法,如分别取等质量等浓度的过氧化氢溶液,依次加入等量、不同种类的催化剂,记录收集等体积氧气所需要的时间。


科目:初中化学 来源: 题型:
【题目】下列用“分子的观点”解释的现象中不正确的是
A.湿衣晾干——分子不停地运动 B.水结成冰——分子发生变化
C.干冰升华——分子间间隔变大 D.热胀冷缩——分子间有间隔
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】分别分解高锰酸钾、氯酸钾、过氧化氢(化学式为H2O2)三种物质,都可以制得氧气.这说明三种物质的组成中都含有( )
A.氧气 B.氧元素 C.氧分子 D.氧化物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某粗盐样品中含有Na2SO4、MgCl2、CaCl2等杂质.实验室提纯流程如下:
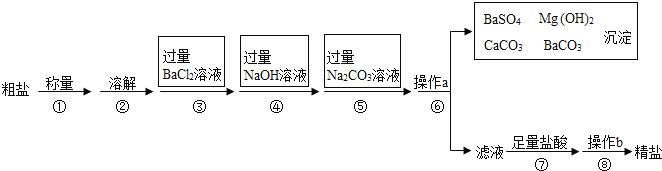
(1)用托盘天平称量粗盐时,若指针偏向右边,则表示(填下列正确选项的代码) .
A.右盘重,砝码轻 B.右盘轻,样品重
C.左盘重,样品轻 D.左盘轻,砝码重
(2)第④步操作发生反应的化学方程式是 .
(3)第⑤步操作的目的是 .
(4)第⑥步操作a的名称是 ,此步操作中,玻璃棒的末端要轻轻地斜靠在 的一边.
(5)在第⑦步操作中,向滤液中滴加足量盐酸的目的是 .
(6)在第⑧步操作时,要用玻璃棒不断搅拌,目的是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯氧化钙是用于电子工业重要的无机化工原料.用硝酸钙溶液制备高纯氧化钙的工艺流程如下:
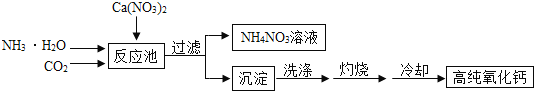
反应池中发生反应的化学方程式为:CO3+2NH3H2O+Ca(NO3)2═2NH4NO3+CaCO3↓+H2O
请回答下列问题:
(1)过滤操作中玻璃棒的作用是 .
(2)过滤后所得沉淀表面可能含有的可溶性杂质有 (写出一种即可).
(3)该工艺流程中可循环使用的物质是 .
(4)冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有的杂质是 .
(5)上述流程中的副产物NH4NO3可用作氮肥,氮肥的主要作用是 .
A、促进植物生长,叶色浓绿
B、增强作物的抗寒,抗旱能力
C、增强作物的抗病虫害和抗倒伏能力.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组按下图所示装置(固定装置已省去)开展有关探究性实验。已知,过氧化氢足量,该装置气密性良好,实验前开关K1和K2均处于关闭状态。实验步骤如下:
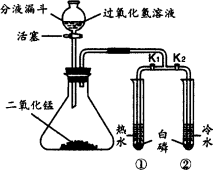
Ⅰ.打开K1、K2,观察现象;
Ⅱ.关闭K1,打开分液漏斗活塞,观察现象;
Ⅲ.打开K1,观察现象;
Ⅳ.回收锥形瓶中的二氧化锰,洗净仪器放回原处。
回答下列问题:
(1)该实验的目的是 ;
(2)步骤Ⅲ观察到试管①中的现象是:有气泡从导管中冒出、 ,试管①中反应的化学方程式为 ,该反应的类型是 反应(填“化合”、“分解”或“置换”);
(3)实验完毕后,回收二氧化锰的实验操作是 、洗涤、干燥;
(4)由步骤Ⅱ、Ⅲ可得出的实验结论是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明发现二氧化锰催化过氧化氢分解的实验中,反应速度逐渐变慢。查阅资料得知:其原因是过氧化氢的溶质质量分数减小以及二氧化锰的催化能力降低。为了探究二氧化锰的催化能力降低的影响因素,进行如下实验。
【材料准备】取质量均为2克的二氧化锰分别催化40毫升溶质质量分数为10%、20%、30%的过氧化氢溶液分解,实验后回收二氧化锰,并分别标为A、B、C;另取多次催化分解10%过氧化氢溶液实验后回收的二氧化锰,标为D。
【实验步骤】
①连接装置并检查气密性。
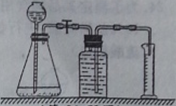
②取未使用过的二氧化锰0.5克,加入锥形瓶中,再加入10毫升溶质质量分数为5%的过氧化氢溶液,记录收集120毫升气体所需的时间。
③在分别取A、B、C、D组二氧化锰0.5克,重复上述实验。
④多次实验取平均值,记录数据如下:
组别 | 未使用过得二氧化锰 | A | B | C | D |
收集气体时间/秒 | 17.9 | 23.2 | 27.7 | 32.3 | 37.8 |
(1)实验时,长颈漏斗下端管口应在液面以下,其目的是 。
(2)实验中通过比较收集相同气体体积所需的时间外,还可以通过比较 来反映二氧化锰的催化能力。
(3)由上表数据可知,引起回收的二氧化锰的催化能力下降的因素是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质的性质与所对应的用途没有直接关系的是
A.干冰升华吸热-----用于人工降雨
B.石墨能导电-----可做铅笔芯
C.焦炭具有还原性-----可用来工业炼铁
D.金刚石硬度大-----可用来切割玻璃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定锌铜合金中锌的含量,取该合金放入如下图盛有稀硫酸的锥形瓶中,发生反应:Zn+H2SO4=ZnSO4+H2↑。多次实验后,取平均值所得数据如下表:
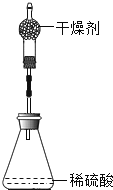
反应前 | 充分反应后装置及反应剩余物质质量 | |
装置和足量的稀硫酸质量 | 锌铜合金质量 | |
342.10g | 16.00g | 357.70g |
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量。
(2)该合金中锌的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com