


 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| [��Ҫ�ɷ�]������������ѧʽ C6H10FeO6?3H2O [�� ��]����������0.3��0.6g/�� [ע������]1���˷���ڷ� 2����ʱ�ɲ裬���ⱻ���ʳ��� [���]0.1g/Ƭ |
| 3Li � 6.941 |
4Be �� 9.012 |
5B �� 10.81 |
6C ̼ 12.01 |
7N �� 14.01 |
8O �� 16.00 |
9F �� 19.00 |
10Ne �� 20.18 |
| 11Na �� 22.99 |
12Mg þ 24.31 |
13Al �� 26.98 |
14Si �� 28.09 |
15P �� 30.97 |
16S �� 32.06 |
17Cl �� 35.45 |
18Ar � 39.95 |
| �й�ָ�� | ��ѧָ�� | ϸ��ѧָ�� |
| ˮ����ɫ��ζ �ҳ����� |
pH6.5��8.5����Ӳ�ȣ�250mg/L ����̼��Ƽƣ���ͭ��1.0mg/L������ |
ϸ��������100��/mL�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| ||
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �μ�������ϡ���� |
| ���� |
| ���� | ���� |
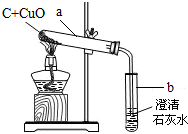
| ��Һ����ɫ���к�ɫ����� | ��CuO��C |
| ��Һ��ɫ�����Ա仯���к�ɫ������ | ֻ���� C C |
| ��Һ����ɫ���� ��ɫ������ ��ɫ������ |
ֻ��CuO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com