
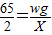 ,
,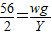
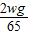 ,Y═
,Y═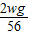 ,
, ,
,
 ,Y═
,Y═ ,
,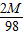 g,
g,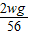 g,
g,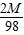 ═
═ 时天平平衡,
时天平平衡, >
>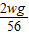 时有铁的一端下沉,
时有铁的一端下沉,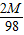 <
<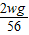 时有锌的一端下沉.
时有锌的一端下沉. ═
═ 时天平平衡,
时天平平衡,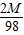 >
> 时有铁的一端下沉,
时有铁的一端下沉, <
< 时有锌的一端下沉.
时有锌的一端下沉.

科目:初中化学 来源: 题型:
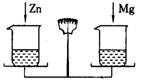
在托盘天平的两个托盘上各放一只烧杯,分别注入相同质量分数、相同质量的稀盐酸,天平平衡。向左边的烧杯中加入1 0 g金属锌,向右边的烧杯中加入1 0 g金属镁。当反应停止后,金属都有剩余,天平指针的指向是
A.分度盘的左边
B.分度盘的中间
C.分度盘的右边
D.3种情况都有可能
查看答案和解析>>
科目:初中化学 来源: 题型:

| A.分度盘的左边 |
| B.分度盘的中间 |
| C.分度盘的右边 |
| D.3种情况都有可能 |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年江苏省盐城市阜宁县九年级下学期第一次学情调研考试化学试卷(解析版) 题型:选择题
在托盘天平的两个托盘上各放一只烧杯,分别注入相同质量分数、相同质量的稀盐酸,天平平衡。向左边的烧杯中加入1 0 g金属锌,向右边的烧杯中加入1 0 g金属镁。当反应停止后,金属都有剩余,天平指针的指向是

A.分度盘的左边
B.分度盘的中间
C.分度盘的右边
D.3种情况都有可能
查看答案和解析>>
科目:初中化学 来源: 题型:单选题

查看答案和解析>>
科目:初中化学 来源:2012届江苏省盐城市阜宁县九年级下学期第一次学情调研考试化学试卷(带解析) 题型:单选题
在托盘天平的两个托盘上各放一只烧杯,分别注入相同质量分数、相同质量的稀盐酸,天平平衡。向左边的烧杯中加入1 0 g金属锌,向右边的烧杯中加入1 0 g金属镁。当反应停止后,金属都有剩余,天平指针的指向是
| A.分度盘的左边 |
| B.分度盘的中间 |
| C.分度盘的右边 |
| D.3种情况都有可能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com