
科目:初中化学 来源: 题型:阅读理解
| 白色粉末的成分 | 形 成 的 原 因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应: 化学方程式为: CO2+Ca(OH)2═CaCO3↓+H2O |
| 可能是 氢氧化钙 |
暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质析出 |
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
| 实 验 步 骤 | 可能观察到的现象 | 结 论 |
| 取上述试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液变红 |
固体中含有氢氧化钙 |
| 往上述试管内残留的固体中加入稀盐酸 | 产生气泡 |
白色粉末中 有 (“有”或“无”)CaCO3 |
| 由上述实验可知白色粉末的成分是: 碳酸钙和氢氧化钙的混合物 | ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 20℃时,一些物质的溶解度 | ||
| OH- | CO32- | |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 实验探究让化学更具魅力,请帮助完成下列实验探究
实验探究让化学更具魅力,请帮助完成下列实验探究| 白色粉末的成分 | 形 成 的 原 因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应: 化学方程式为: CO2+Ca(OH)2=CaCO3↓+H2O CO2+Ca(OH)2=CaCO3↓+H2O |
| 可能是 Ca(OH)2 Ca(OH)2 |
随着气温的升高,溶质的溶解度会 变小 变小 填变大或变小)或溶剂蒸发,石灰水中的溶质析出 |
| 实 验 步 骤 | 可能观察到的现象 | 结 论 |
| 取上述试管中的上层清液,滴加1~2滴无色酚酞试液 | 溶液变红 | 白色粉末中含Ca(OH)2 白色粉末中含Ca(OH)2 |
| 往上述试管内残留的固体中加入稀盐酸 | 产生气泡 产生气泡 |
白色粉末中含有CaCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(四川成都卷)化学(解析版) 题型:探究题
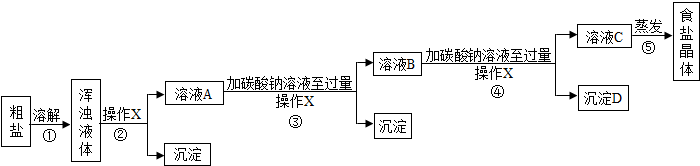
通过晾晒海水或煮盐井水、盐湖水等,可以蒸发除去水分得到粗盐。粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。
[提出问题]如何才能将粗盐中难溶性杂质和可溶性杂质(氯化镁、氯化钙)除去,从而获得较纯的食盐晶体?
[资料准备]
|
20℃时,一些物质的溶解度 |
||
|
|
OH- |
CO32- |
|
Na+ |
溶 |
溶 |
|
Ca2+ |
微 |
不 |
|
Mg2+ |
不 |
微 |
[实验方案]某同学为了提纯粗盐,设计了如下实验方案并进行实验。
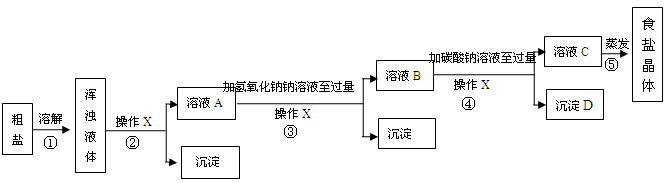
[交流与表达]
(1)实验步骤①和②的目的是 ;实验步骤③和④的目的是 。
(2)实验操作X的名称是 ,该操作中要用到的玻璃仪器有烧杯、玻璃棒和 。
(3)实验步骤③的主要目的是 (用化学方程式回答);判断氢氧化钠溶液已过量的方法是 。
(4)实验步骤④中生成的沉淀D是 。
(5)实验步骤⑤用蒸发溶剂的方法而不用降低溶液温度的方法获取食盐晶体,原因是 ;在蒸发食盐溶液的过程中要使用玻璃棒,作用是 。
[反思与评价]
(6)有同学认为只需要用氢氧化钠溶液和碳酸钠溶液中任意一种试剂就能将两种可溶性杂质出去,你认为这种方法 (选填“可行”或“不可行”),理由是 。
(7)有同学认为原实验方案不完善,做出这种评价的依据是 。
[实验方案设计]
(8)为了完善原实验发难,你设计的实验是 (仅写出补充部分的实验操作和现象)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com