
 如图是测定空气中氧气体积分数的实验装置示意图,已知集气瓶容积约为80mL,实验结束时流入集气瓶中水的体积约为16mL.下列有关说法错误的是( )
如图是测定空气中氧气体积分数的实验装置示意图,已知集气瓶容积约为80mL,实验结束时流入集气瓶中水的体积约为16mL.下列有关说法错误的是( )| A. | 燃烧结束,等集气瓶冷却到室温后松开弹簧夹读数 | |
| B. | 本实验中,测出空气中氧气的体积分数约为1/5 | |
| C. | 流入集气瓶中水的体积约等于磷燃烧消耗氧气的体积 | |
| D. | 可以用木炭代替红磷测定空气中氧气的体积分数 |
分析 测定空气中氧气含量的实验结论是氧气约占空气体积的五分之一,要想结论准确,做该实验时,装置的气密性要好;药品的量要足,把氧气全部耗尽;等到装置冷却到室温再打开弹簧夹读数等等.燃烧结束后立刻打开弹簧夹,测量的结果会小于五分之一.
解答 解:A.等到装置冷却到室温再打开弹簧夹读数,而不能红磷熄灭后立即打开弹簧夹,否则会使得结果小于五分之一,故正确;
B.本实验中,测出空气中氧气的体积分数约为$\frac{16mL}{80mL}×100%=20%$,即空气中氧气的体积分数约为$\frac{1}{5}$,故正确;
C.测定空气中氧气含量实验是红磷燃烧消耗掉氧气,导致装置内压强减小,打开弹簧夹,水会倒流进瓶内,因此最终进入瓶中水的体积约为氧气的体积,故正确;
D.木碳燃烧生成二氧化碳气体,装置内气体的压强不变,所以无法测定空气中氧气的含量,故错误.
故选D.
点评 该题主要考查测定空气里氧气含量的探究实验,该实验的结论、误差分析和实验中注意事项是考查重点.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开盛浓盐酸的瓶塞有白烟生成 | |
| B. | 黄色pH试纸条沾到碱液变红色 | |
| C. | 氢氧化钠溶液中滴加硫酸铜溶液有蓝色沉淀生成 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成四氧化三铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种,某实验小组对其组成成分进行了以下探究活动.
有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种,某实验小组对其组成成分进行了以下探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
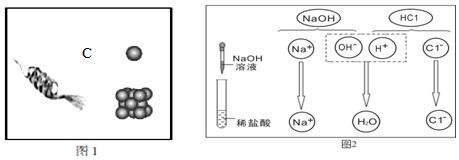

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图是部分含碳物质的转化关系图,根据图示回答下列问题.
如图是部分含碳物质的转化关系图,根据图示回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 证明铜比银活泼:Cu+2AgCl═CuCl2+2Ag | |
| B. | 酸雨的形成原理:CO2+H2O═H2CO3 | |
| C. | 盐酸除铁锈(Fe2O3•nH2O):Fe2O3•nH2O+6HCl═2FeCl3+(n+3)H2O | |
| D. | 除去H2中混有的HCl气体:Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一种原子只能构成一种分子 | |
| B. | 质子数相等的粒子一定属于同种元素 | |
| C. | 原子得失电子形成离子时,其电子层数可能有变化 | |
| D. | 同种元素的粒子,其核外电子数一定相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com