

分析 Ⅰ.根据物质的性质及作用解答;
Ⅱ.①根据主要成分的化学式来分析;
②结合n=$\frac{N}{{N}_{n}}$、m=nM及分子构成计算.
Ⅲ.根据化学方程式来分析解答;
Ⅳ.①镁与二氧化碳反应生成氧化镁和碳;
②根据在化学变化中元素质量守恒来分析.
解答 解:
Ⅰ.①日常生活中用作溶剂的是水;通过物理方法可提取氧气的是空气.利用分离液态空气的方法制取氧气;
②生活中常用作建筑材料的是大理石;属于清洁的气体矿物燃料的是天然气;
Ⅱ.①A.主要成分中含有两种元素;B.主要成分中含有四种元素;C.主要成分中含有三种元素;D.主要成分中含有两种元素;故填:B;
②SiO2的摩尔质量为60g/mol;n(Si)=$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}}$=0.5mol,则n(SiO2)=0.5mol,其质量为0.5mol×60g/mol=30g;
Ⅲ.设:三种物质的量均为xmol,
①甲烷完全燃烧需要氧气物质的量为a,CH4燃烧的方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
1 1
xmol a
a=xmol
②C2H2完全燃烧需要氧气物质的量为b,燃烧的方程式为:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O
2 5
xmol b
b=2.5mol
③C2H4完全燃烧需要氧气物质的量为c,燃烧的方程式为:C2H4+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2H2O
1 3
xmol c
c=3xmol
答案:③②①
Ⅳ.①金刚石的主要成分是碳,碳与氧气在点燃的条件下生成二氧化碳;镁与二氧化碳反应生成氧化镁和碳,步骤b中发生反应的化学方程式为:2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$ C+2MgO;
(2)在化学变化中元素质量守恒,故金刚石的质量就等于生成碳粉的质量.
答案:
Ⅰ.①水;空气;②大理石; 天然气;
Ⅱ.①B; ②60g/mol;0.5;30;
Ⅲ.③②①;
Ⅳ.①2Mg+CO2 $\frac{\underline{\;点燃\;}}{\;}$ C+2MgO;
②=;化学反应中元素质量守恒.
点评 本题难度不大,考查同学们灵活运用化学式和化学方程式的有关计算进行分析问题、解决问题的能力.要注意用简便的方法来解决实际问题.考查的是质量守恒定律的应用,解题的关键是灵活运用质量守恒定律.


科目:初中化学 来源: 题型:选择题
| A. | 发现家里煤气泄露时,立即打开排气扇 | |
| B. | 硫酸铜溶液不能用铁质容器盛放 | |
| C. | 家用铝锅不宜用铁丝球用力擦洗 | |
| D. | 实行垃圾分类回收,既节约资源,又保护环境 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
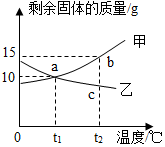 将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )
将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,剩余固体物质与温度的关系如图所示,下列说法正确的是( )| A. | 甲的溶解度随温度升高而增大 | |
| B. | t1℃时,甲、乙的溶解度均为20g/100g水 | |
| C. | 温度由t2℃降低到t1℃时,甲溶液析出5g固体 | |
| D. | a、b、c三点中溶质的质量分数由大到小的顺序是c>a>b |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2都有 |

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
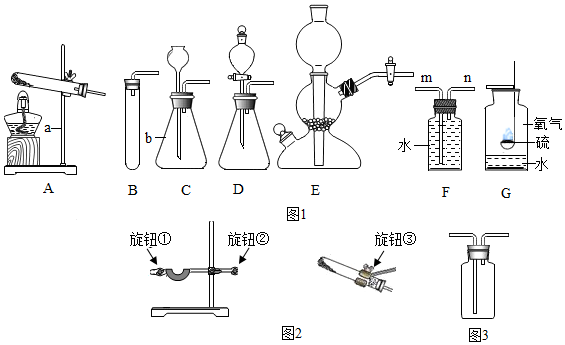
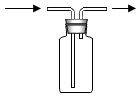 .
.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
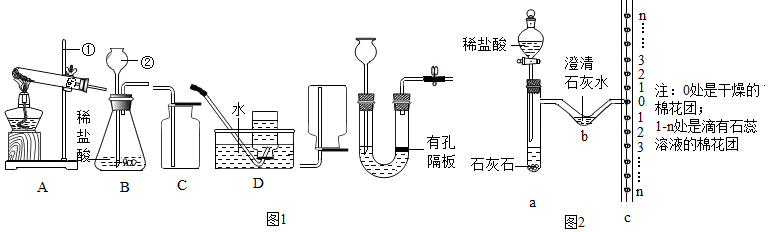

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com