
| 现象 | 分析 |
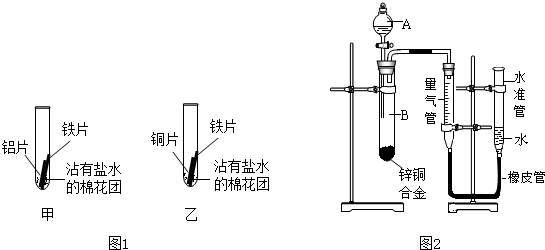
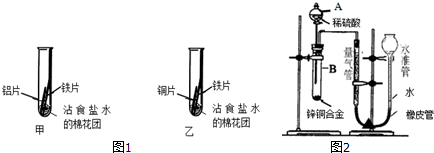
| 甲中:铝片表面出现灰白色物质,铁片表面几乎没有明显现象. | 铝与铁在潮湿的环境中接触,______首先被腐蚀. |
| 乙中:铁片表面出现______,铜片表面几乎没有明显现象. | 铁与铜在潮湿的环境中接触,铁首先被腐蚀. |
| 65 |
| x |
| 2 |
| 0.00765g |
| 0.145g |
| 0.561g |


科目:初中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取一定量的草木灰于烧杯中,加入适量蒸馏水,搅拌,然后进行______操作. | 得到无色溶液 | |
| (2)取少量无色溶液于试管中,然后滴加几滴酚酞试液 | 溶液变红色 | 溶液显______性. |
| (3)取少量无色溶液于试管中,然后加入少量______; | 有______产生; 澄清石灰水______ | 有______生成, 草木灰的主要成分是碳酸钾,猜想(2)成立 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
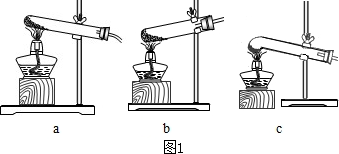
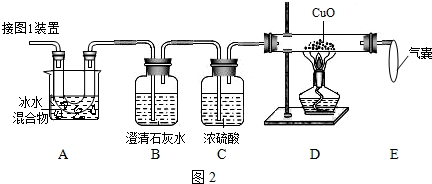
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
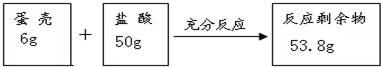
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 实验序号 | 实验操作 | 实验现象 | 解释及结论 |
| 实验I | 用砂纸擦去镁条表面氧化膜,将其放入盛有适量饱和碳酸氢钠溶液的试管中 | 迅速反应,产生大量气泡和白色不溶物 |  |
| 实验Ⅱ | 将实验I中收集到的气体点燃,并在火焰上方罩一干、冷的小烧杯 | 气体安静燃烧、产生淡蓝色火焰,烧杯内壁有水雾出现. | 该气体是______,燃烧的化学方程式为 ______. |
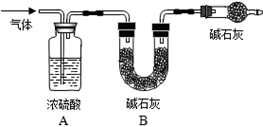
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 方案 | 实验假设 | 实验方案 | 实验现象与结论 |
| Ⅰ | 能发生钝化 | 取一铁片先插入浓硫酸中,一段时间后取出,再插入硫酸铜溶液中. | 无明显变化,假设成立. |
| Ⅱ | 能发生钝化 | 取两片相同的铁片,一片放入浓硫酸中,一段时间后取出,与另一片同时放入硫酸铜溶液中. | ______,假设成立. |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
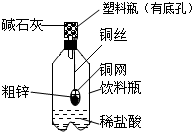
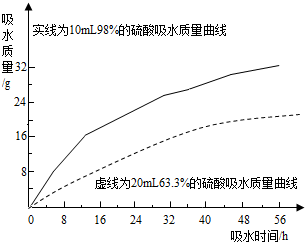
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com