
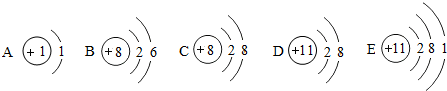
| ||
| ||


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
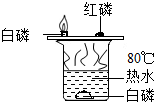 课堂上老师曾经给我们演示了如图所示的实验,请回答下列问题(温馨提示:白磷的着火点为40℃,红磷的着火点为240℃):
课堂上老师曾经给我们演示了如图所示的实验,请回答下列问题(温馨提示:白磷的着火点为40℃,红磷的着火点为240℃):查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
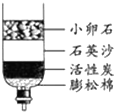 化学是研究物质的组成、结构、性质及其变化规律的基础自然科学,请回答下列问题:
化学是研究物质的组成、结构、性质及其变化规律的基础自然科学,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
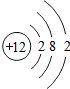 如图是某元素的原子结构示意图,该原子的核电荷数是
如图是某元素的原子结构示意图,该原子的核电荷数是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com