
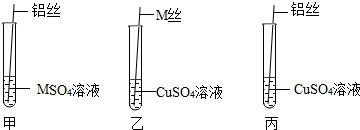
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu:M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
分析 【提出问题】根据其余两种猜想推断第三种猜想;
【设计与实验一】根据金属与酸反应的剧烈程度进行分析;
【交流与表达】根据铝和空气中的氧气反应会生成致密的氧化铝薄膜进行分析;
【设计与实验二】(1)根据M的金属活动性大于铜的金属活动性进行分析;
(2)根据铝和硫酸铜反应生成硫酸铝和铜进行分析;
【交流与表达】根据甲、乙、丙三个实验得出的金属活动性顺序进行分析;
【评价与反思】根据金属会与酸、盐、氧气等物质反应进行分析.
解答 解:【提出问题】通过分析小敏、小强同学的猜想可知,我的猜想是M>Al>Cu;
【设计与实验一】金属越活泼,与酸反应生成氢气的反应越剧烈,所以
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu,M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| M>Al | ||||
| Al>M>Cu |
点评 验证三种金属活动性强弱关系时,通常采取“三取中”即:取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 0.5g | B. | 4.5g | C. | 5.6g | D. | 5g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁带在空气中燃烧;酒精挥发 | |
| B. | 二氧化硫具有刺激气味;氯气有毒 | |
| C. | 氧气能支持燃烧;水在降温时会结冰 | |
| D. | 蜡烛受热熔化;液氧是淡蓝色的液体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 纸不是可燃物 | B. | 汤料降低了纸的着火点 | ||
| C. | 汤料有吸热降温的作用 | D. | 纸没有与氧气接触 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
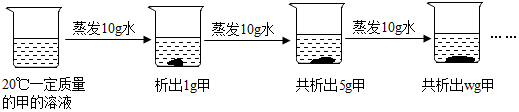
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳纳米管的体积在 10℃至 500℃之间随温度变化很小,可忽略不计 | |
| B. | 金属镓的熔点、沸点都很低 | |
| C. | 在 30℃至 490℃之间金属镓的体积与温度变化呈正比 | |
| D. | 金属镓的体积在 30℃至 490℃之间随温度变化很小,可忽略不计 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com