
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想猜想三不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 有气泡产生 | 猜想二成立 |
分析 根据氢化钙(CaH2)与水的反应写出反应的化学方程式;
【猜想与假设】根据氢氧化钙与碳酸钠的反应及反应物的量,对反应后的溶液溶质进行猜想;
【实验验证】实验一、根据碳酸钠与氢氧化钙的反应分析;
实验二、根据碳酸钠与稀盐酸的反应分析;
【反思与拓展】①根据氢化钙(CaH2)与水反应的产物、产物与氯化铵的反应分析生成的气体;
②比较CaH2、氢气的特点分析回答;
【定量分析】根据反应的方程式,由碳酸钙的质量求出氢化钙的质量及质量分数.
解答 解:由题意可知,氢化钙(CaH2)与水反应生成氢氧化钙和氢气,反应的方程式是:CaH2+2H2O=Ca(OH)2+2H2↑;
【猜想与假设】由于氢化钙(CaH2)与水反应生成氢氧化钙和氢气,碳酸钠与氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,所以猜想三是:氢氧化钠,氢氧化钙;因为碳酸钠与氢氧化钙不能共存,所以猜想一是不合理的,方程式是:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
【实验验证】在实验①中,由滤液中滴入少量碳酸钠溶液,无明显现象,说明没有氢氧化钙,即猜想三不成立;实验②:由向滤液中加入足量稀盐酸,若观察到无气泡的现象时,说明滤液中不含有碳酸钠,即猜想二成立;
【反思与拓展】
①由于氢化钙(CaH2)与水反应生成了氢氧化钙和氢气,氢氧化钙与氯化铵反应生成了氯化钙、氨气和水,所以,产生的气体是NH3,H2;
②CaH2作为能源提供剂,与氢气相比,其优点是固体便于携带;
设氢化钙样品中氢化钙的质量为x
由CaH2+2H2O=Ca(OH)2+2H2↑
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
可得出:
CaH2~CaCO3
42 100
x 20g
$\frac{42}{100}=\frac{x}{20g}$ 解得:x=8.4g
氢化钙样品中氢化钙的质量分数为:$\frac{8.4g}{10g}$×100%=84%
【猜想与假设】氢氧化钠,氢氧化钙,猜想一,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
【实验验证】猜想三不成立,有气泡产生;
【反思与拓展】NH3,H2,固体便于携带,(安全)
【定量分析】氢化钙样品中氢化钙的质量分数是84%
点评 实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:选择题
| A. | 液氧 熟石灰 空气 | |
| B. | 活性炭 酒精 碘盐 | |
| C. | 生铁 干冰 矿泉水 | |
| D. | 金刚石 冰 高锰酸钾制氧气的剩余固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 烧杯 | 烧杯 | 烧杯 | 烧杯 | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 |
| 充分反应后生成气体的质量/g | 0.88 | 1.76 | 2.64 | 2.64 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2(CO) | 足量O2 | 点燃 |
| B | NaCl(NaOH) | 过量的稀盐酸 | 蒸发结晶 |
| C | HCl(CO2) | 适量NaOH溶液 | 洗气 |
| D | 稀盐酸(稀硫酸) | 适量硝酸钡溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 倾倒液体时,试剂瓶口紧挨着试管口快速倒入 | |
| B. | 加热蒸发过程中,当溶液蒸干时停止加热 | |
| C. | 用pH试纸测定溶液的酸碱度时,将pH试纸放入待测液中蘸取 | |
| D. | 过滤时,漏斗中液面低于滤纸的边缘 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
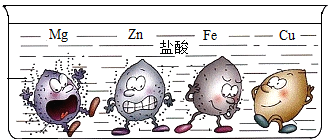 教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示:
教材上有一幅很形象的卡通画表示金属与盐酸的反应现象.卡通人物表示一种金属,周围的小黑点表示反应中生成的气体,如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验用剩的药品应放回原试剂瓶中 | |
| B. | 过滤时,将玻璃棒靠在三层滤纸的一边 | |
| C. | 测某酸性溶液的pH时,先用水将pH试纸润湿 | |
| D. | 把烧杯置于铁架台的铁圈上直接加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com