(1)“爆竹声中一岁除”燃放烟花爆竹是中华民族文化的重要组成部分,然而,近年灰我国许多大、中城市都对烟花爆竹实施了“禁放“或者”限放“,民族文化为什么受到限制,好奇心驱使小明,小强、小亮三位同学,他们决定对烟花爆竹进行展开实验探究.

[提出问题]烟花爆竹燃放时会产生什么气体?
[查阅资料]我国传统的黑火药的标准配方为:硝酸钾75%、硫磺l0%、木炭l5%,因为黑火药中的硫磺成分具有着火温度低、燃速快等性质,因而使黑火药容易点火,使得在生产过程中硫的使用量过大.
(2)CO
2和SO
2均能使石灰水变浑浊;
[猜想]烟花爆竹燃放时会产生CO
2和SO
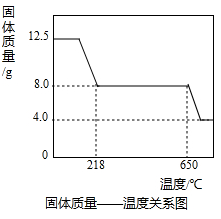
2[实验过程]他们设计的实验探究过程如图1实验开始前应先检查
气密性
气密性
,再点燃酒精灯,已知2处为从爆竹中取出的少量的火药,根据实验设计要求应当还要用到
紫红
紫红
色的高锰酸钾溶液和石灰水,则3中应放的是
高锰酸钾
高锰酸钾
,4中应放的是
澄清石灰水
澄清石灰水
,若猜想正确,4中发生反应的化学方程式是
Ca(OH)2+CO2=CaCO3↓+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
.结果证明原猜想正确,
[实验反思]
(1)装置中气球的作用是
起到实验时对气体的缓冲作用
起到实验时对气体的缓冲作用
,
(2)已知 硬质玻璃管中发生的反应有S+2KNO
3+3C═3CO
2+N
2+X,则X的化学式为
K2S
K2S
.该玻璃管中还发生的反应
(写化学方程式)搞清烟花爆竹的基本原理和实验中产生的气体之后,该兴趣小组又利用春节期间测定市区某烟花爆竹集中燃放点处二氧化硫的含量
[查阅资料]可用含有一定量碘的溶液测定空气中的SO
2含量,反应方程式是:SO
2+I
2+2H
2O=H
2SO
4+2HI.
[测定装置]:甲同学设计了如图2所示的实验装置:
[测定步骤]:
(一) 配制一定浓度的稀碘溶液
(二)二氧化硫含量的测定
(1)将一定浓度、一定质量的稀碘溶液放于洗气瓶中,并滴入几滴稀淀粉溶液,此时洗瓶中溶液的颜色为蓝色.(淀粉遇碘单质呈蓝色)
(2)3位同学分别设计好的装置来到燃放点,打开a,关闭b用注射器抽取100mL燃放点空气.再关闭a,打开b,再缓缓推动注射器,将气体全部推入滴有淀粉的碘水溶液中,重复上述操作多次,直到溶液刚好变成无色,记录抽气的次数
(3)3位同学使溶液刚好变成无色时抽气的次数分别为50、60、65次,
50
50
次的最接近真实值,另两位同学不准确的原因为
二氧化硫未能与溶液充分反应
二氧化硫未能与溶液充分反应
(4)最终我们通过计算可以确定燃放点的二氧化硫含量是否超标.
[测定反思]
(1)小明经过思考后认为在测定时可将图3所示的多孔球泡放入洗气瓶中,你认为加此仪器的好处是
增加了反应物的接触面积,使反应更加充分
增加了反应物的接触面积,使反应更加充分
.
(2)小强同学认为:实验方案需要抽气的次数太多,操作麻烦.与小亮讨论后,决定对设计的实验加以调整,以减少抽气的次数,他们调整的方案可能是
减少碘液的量
减少碘液的量
.
(3)三位同学经过对烟花爆竹的研究,明白了国家“禁放”的和“限放”的原因,你认为原因的是
A、B、C、D
A、B、C、D
A 减少噪声污染 B 减少固体废弃物污染 C 减少大气污染 D 减少粉尘污染.




 一本好题口算题卡系列答案
一本好题口算题卡系列答案
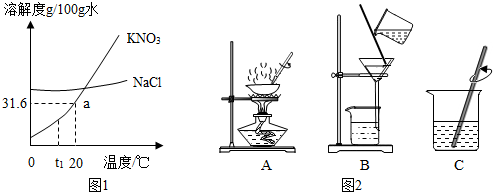

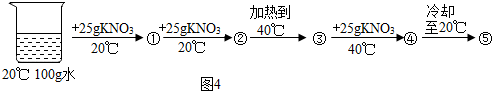
 KNO3、NaCl溶液在生产、生活中起着十分重要的作用.如图是它们的溶解度曲线,下表是它们在不同温度时的溶解度.
KNO3、NaCl溶液在生产、生活中起着十分重要的作用.如图是它们的溶解度曲线,下表是它们在不同温度时的溶解度.