

���� ���������Ӻ�̼������ӷ�Ӧ�����ɶ�����̼���壬�����Ӻ������ӷ�Ӧ�����Ȼ����������з�����
��1������ϡ�������������Ӧ������������ˮ�����������Ȼ�����Ӧ�������ᱵ�������Ȼ������Ȼ���Ҳ����ϡ���ᷴӦ�������ᱵ���������ᣬa��b�γ�������û�����Ա仯������һ����������������Ƶķ�Ӧ��������������������Ƶķ�Ӧ������A�Թܵ�������һ���������ᡢ���������з�����
��2���������е�ʵ��������з�����
��� �⣺�����Ӻ�̼������ӷ�Ӧ�����ɶ�����̼���壬�����Ӻ������ӷ�Ӧ�����Ȼ�������������ͼ1ʵ�飬��ȷ��X�����ᣬ��Y������̼������Һ��
��1��ϡ�������������Ӧ������������ˮ�����������Ȼ�����Ӧ�������ᱵ�������Ȼ������Ȼ���Ҳ����ϡ���ᷴӦ�������ᱵ���������ᣬa��b�γ�������û�����Ա仯������һ����������������Ƶķ�Ӧ��������������������Ƶķ�Ӧ������A�Թܵ�������һ���������ᡢ����������ѧʽΪ��H2SO4��Fe2��SO4��3��ʵ���У�?A�з����ķ�Ӧ�������������ᷴӦ������������ˮ����ѧ����ʽΪ��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��a��b�ζ�Ӧ��Һ��һ�������ķ�Ӧ���������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ����ѧ����ʽΪ��?NaOH+HCl=NaCl+H2O������c���Ӧ��Һ�к������ʿ��ܵ�����У�?NaCl��NaCl��BaCl2��NaCl��Na2SO4��
��2��ͨ�����������ᷢ���ķ�Ӧ��֪����Ļ�ѧ�����У��������Ρ�����������Ӧ��
�ʴ�Ϊ����1��̼������Һ��
��2��H2SO4��Fe2��SO4��3?��Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
?NaOH+HCl=NaCl+H2O��?NaCl��NaCl��BaCl2��NaCl��Na2SO4��
��3���������Ρ�����������Ӧ��
���� ������Ҫ��������Ļ�ѧ���ʣ��ѶȲ�����Ҫ��ƽʱ��ѧϰ�м�ǿ���伴����ɣ�


 ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д� ����˼ά�żӿ���ϵ�д�
����˼ά�żӿ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
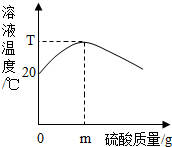 20��ʱ��������粻���������������ܱ������У���400g 10%������������Һ��ϡ�����ϣ���Ӧ��������Һ�¶�������������ϵ��ͼ������˵����ȷ���ǣ�������
20��ʱ��������粻���������������ܱ������У���400g 10%������������Һ��ϡ�����ϣ���Ӧ��������Һ�¶�������������ϵ��ͼ������˵����ȷ���ǣ�������| A�� | ������������m��ʱ���ܱ������ں��е�������������������� | |
| B�� | ��������С��m��ʱ���ܱ������ں��е������������������ | |
| C�� | ����Ũ�������ϡ���ᣬ��ǡ�÷�Ӧʱ��Һ�¶ȵ���T�� | |
| D�� | ����40g�������ƹ����������������Һ����ǡ�÷�Ӧʱ��Һ�¶ȸ���T�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͬѧ��pH��ֽ�����ˮ��pH=5.6 | |
| B�� | ��ͬѧ��������ƽ������ֽ�ϳ���NaOH���� | |
| C�� | ��ͬѧ������������ȼ��ʵ��ʱ�۲쵽����������ȼ�գ��������䣬�ų��������ȣ����ɺ�ɫ������������ | |
| D�� | ��ͬѧ�ڡ�ʵ������ȡ��������ʵ��ʱ��������غ�����ػ�ϼ�����ȡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ǻ����� | |
| B�� | ��������5��Ԫ����� | |
| C�� | ��������C��HԪ�ص���������13��16 | |
| D�� | ������һ�����Ӻ���32��ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
| ���� | ��һ�� | �ڶ��� | ������ |
| ����ϡ��������/g | 5 | 5 | 5 |
| ������������/g | 0.02 | 0.02 | 0.01 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ̽������ȼ�յ����� | |
| B�� | 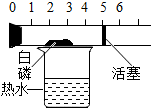 ̽�������������ĺ��� | |
| C�� |  ̽����Ӧ��Ӵ�����Է�Ӧ���ʵ�Ӱ�� | |
| D�� | 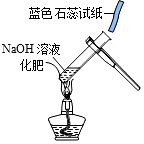 ̽��ij�����Dz����̬���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cu$\stackrel{����}{��}$CuCl2$\stackrel{��������}{��}$Cu��OH��2 | |
| B�� | Cu$\stackrel{����п}{��}$CuSO4$\stackrel{��������}{��}$Cu��OH��2 | |
| C�� | Cu$��_{��}^{����}$CuO$\stackrel{����}{��}$CuSO4$\stackrel{��������}{��}$Cu��OH��2 | |
| D�� | Cu $��_{��}^{Ũ����}$ CuSO4$\stackrel{��������}{��}$Cu��OH��2��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com