

分析 (1)根据元素周期表的信息来分析;
(2)金属元素的名称汉字是钅字旁;
(3)根据元素是具有相同核电荷数(即核内质子数)的一类原子的总称,进行解答本题.
(4)根据元素组成物质及化学式的书写方法解答.
解答 解:(1)据表格可以查得铝元素的相对原子质量为26.98,故填:26.98;
(2)11~18号元素中属于金属元素的是钠元素、镁元素和铝元素,故填:Na、Mg、Al;
(3)根据元素的概念,元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的微粒是质子数即元素的最本质区别是质子数不同.故填:A.
(4)6、8、11号元素分别为碳、氧、钠,三者可组成碳酸钠,故填:Na2CO3.
点评 本题考查了元素周期表中信息的应用,元素的定义及化学式的书写,属于基础知识考查.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
| 石蜡 | 50∽70 | 300∽550 | 约600 |
| 铁 | 1535 | 2750 | 约1800 |
| 钠 | 97.8 | 883 | 约1400 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
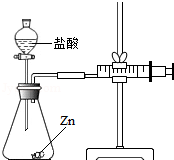 化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.
化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究.| 实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1-2分钟 | 2-3分钟 | 3-4分钟 | 4-5分钟 | 前5分钟共收集气体 | |||
| Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.0 | 9.2 | 7.6 | 48.5 |
| Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com