
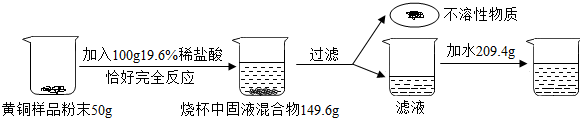
���� ��1��������Һϡ��ǰ��������������������з�����
��2������п��ϡ���ᷴӦ��������п���������з�����
��3������п��ϡ���ᷴӦ��������п�����������ݲμӷ�Ӧ��������������μӷ�Ӧ��п��������
��4�����ݼ������п����������ͭ������������
��5�����ݻ�ѧ����ʽ�������ɵ�����п��Ȼ���������������Һ�����ʵ�����������
��� �⣺��1����Ҫ��������Ϊ98%��Ũ����������ǣ�$\frac{100g��19.6%}{98%}$=20g��
��2��п��ϡ���ᷴӦ��������п��������ѧ����ʽΪ��Zn+H2SO4=ZnSO4+H2����
��3����μӷ�Ӧ��п������Ϊx����������п������Ϊy��������������Ϊz
Zn+H2SO4=ZnSO4+H2��
65 98 161 2
x 100g��19.6% y z
$\frac{65}{x}=\frac{98}{100g��19.6%}=\frac{161}{y}=\frac{2}{z}$
x=13g
y=32.2g
z=0.4g
��4����ͭ��Ʒ��ͭ�����������ǣ�$\frac{50g-13g}{50g}$��100%=74%��
��5������������Һ�����ʵ���������Ϊ��$\frac{32.2g}{100g+13g+209.4g-0.4g}$��100%=10%��
�ʴ�Ϊ����1��20g����2��Zn+H2SO4=ZnSO4+H2����
��3��$\frac{65}{x}=\frac{98}{100g��19.6%}$��
��4��74%��
��5��10%��
���� ������Ҫ�����˻�ѧ����ʽ�ļ��㣬�ѶȲ���ע�����Ĺ淶�ԣ�


 ѧ���쳵�����ּ��������ҵ�½����������ϵ�д�
ѧ���쳵�����ּ��������ҵ�½����������ϵ�д� �����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӵ������㽭��ѧ������ϵ�д� Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
Сѧ�����ҵ���ϴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe+2HCl�TFeCl2+H2�� | B�� | C+2CuO$\frac{\underline{\;����\;}}{\;}$2Cu+CO2�� | ||
| C�� | Fe+CuSO4�TCu+FeSO4 | D�� | 3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | �������� | �Ȼ��� |
| ˮ���� | ���ܣ���15��ʱ100gˮ���ܽ���������81.5g | ���ܣ���15��ʱ100gˮ���ܽ��Ȼ���35.8g |
| �۵� | 271�� | 801�� |
| �е� | 320���ֽ⣬�ų��г�ζ������ | 1 413�� |
| ��ϡ���ᷴӦ | �ų�����ɫ������������� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʱ�ò������������©����Һ�壬�Լӿ�������� | |
| B�� | ����������Ϊ8������һ����ϡ������Ԫ�ص�ԭ�� | |
| C�� | ��ԭ��ʧȥ��õ����Ӻ������ʷ����˸ı䣬����������Ԫ�������ı� | |
| D�� | ��ȡ��߸�ţ�̡��ɸ����岹�ƣ�����ġ��ơ�Ӧ����Ϊԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͼ��ʾ�������巢����ѧ��Ӧ��������ͬ�������ͬ��ԭ�ӣ�����ͼʾ��Ϣ���ж�����˵����ȷ����C
��ͼ��ʾ�������巢����ѧ��Ӧ��������ͬ�������ͬ��ԭ�ӣ�����ͼʾ��Ϣ���ж�����˵����ȷ����C�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������һ�ֻ����� | |
| B�� | ��������̼���⡢��ԭ�Ӹ�����15��22��5 | |
| C�� | �����ص���Է�������Ϊ282 | |
| D�� | ��������̼Ԫ�ص���������С����Ԫ�ص��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ������������ȼ�ղ����������� | |
| B�� | ��˿��������ȼ�գ��������䣬���ɺ�ɫ���� | |
| C�� | ľ̿��������ȼ�գ�������ɫ���� | |
| D�� | ����ͭ��ʱ����ɫ��ĩ��Ϊ��ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ȼ������������ȼ�ղ��������İ��������� | |
| B�� | þ���ڿ�����ȼ�շ���ҫ�۵İ⣬���ɰ�ɫ���� | |
| C�� | ����ͭ�̣���ɫ��ĩ���ɺ�ɫ | |
| D�� | ��ͭ˿������������Һʱ��ͭ˿�����������ɫ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com