
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
分析 【操作分析】根据金属的表面可能有与氧气反应生成的氧化物或污物进行分析;
【实验结论】(1)根据在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,且金属活动性越强,反应越剧烈进行分析;
(2)由(1)中的分析,确定三种金属的活动性顺序即可;
【结论应用】根据铝的活动性比铜强,铝制容器能与硫酸铜溶液发生置换反应进行分析.
解答 解:【操作分析】金属的表面可能有与氧气反应生成的氧化物或污物,用砂纸打磨三种金属,其目的是除去三种金属表面的氧化物或污物,利于直接反应;
【实验结论】(1)Ti与盐酸反应缓慢,铝与盐酸反应剧烈,Cu与稀盐酸无明显现象,说明铝的活动性最强,钛其次,铜活动性最弱,故a假设错误;
(2)三种金属的金属活动性由强至弱的顺序为A1、Ti、Cu;
【结论应用】铝的活动性比铜强,铝制容器能与硫酸铜溶液发生置换反应,生成硫酸铝和铜,化学方程式为:2Al+3CuSO4═Al2(SO4)3+3Cu.
故答案为:【操作分析】A;
【实验结论】(1)a;
(2)A1、Ti、Cu;
【结论应用】否,2Al+3CuSO4═Al2(SO4)3+3Cu.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.


 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案 小天才课时作业系列答案
小天才课时作业系列答案科目:初中化学 来源: 题型:解答题
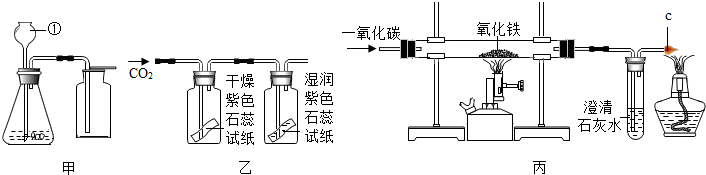
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 气体名称 | 收集方法 | 检验方法 |
| 氧气 | 排水法或向上排空气法收集 | 将带火星的木条放在导管口,若木条复燃证明是氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
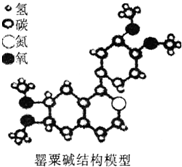 毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )
毒品是全球性公害,是人类共同的敌人.罂粟碱即是其中的一种,从组成和结构认识罂粟碱叙述正确的是( )| A. | 罂粟碱是由四种原子构成的有机物 | |
| B. | 罂粟碱分子中含有4种原子 | |
| C. | 罂粟碱中氮、氧元素的质量比为1:4 | |
| D. | 罂粟碱中氢原子与碳原子的个数比为19:21 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
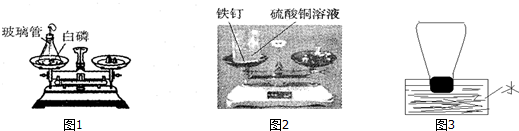
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com