
| A. | 过氧乙酸中含有氧分子 | |
| B. | 过氧乙酸由碳、氢、氧三种原子构成 | |
| C. | 完全燃烧时生成二氧化碳和水 | |
| D. | 过氧乙酸中氢元素、氧元素的质量比为4:3 |
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:初中化学 来源: 题型:解答题
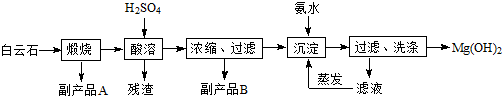
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
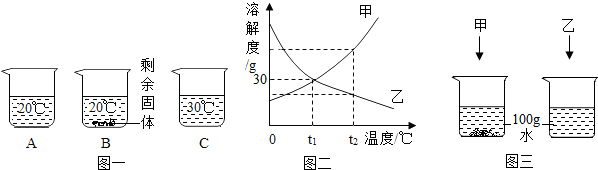
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
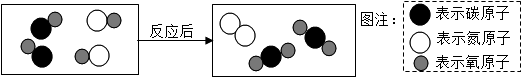
| A. | 参加反应的物质分子个数比为1:1 | |
| B. | 该反应为置换反应 | |
| C. | 生成物的质量比为7:22 | |
| D. | 反应物均为氧化物且该反应遵循质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 生铁、碳酸钙、矿泉水 | B. | 氢气、乙醇、石油 | ||
| C. | 氨气、葡萄糖、冰水共存物 | D. | 红磷、一氧化碳、空气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定含有碳、氢两种元素,一定没有氧元素 | |
| B. | 一定含有碳、氧两种元素,一定没有氢元素 | |
| C. | 一定含有碳、氢两种元素,可能含有氧元素 | |
| D. | 一定含有碳、氢、氧三种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
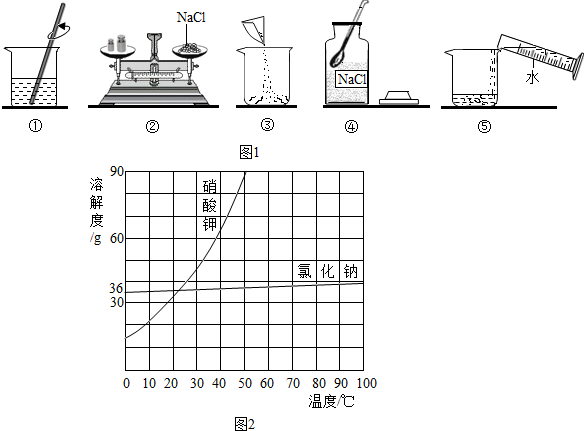
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com