
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ł¢Ś¢Ū | C£® | ¢Ł¢Ū¢Ü | D£® | ¢Ł¢Ś |
·ÖĪö æÕĘųĪŪČ¾µÄĶ¾¾¶Ö÷ŅŖÓŠĮ½øö£ŗÓŠŗ¦ĘųĢåŗĶ·Ū³¾£®ÓŠŗ¦ĘųĢåÖ÷ŅŖÓŠŅ»Ńõ»ÆĢ¼”¢¶žŃõ»ÆĮņ”¢¶žŃõ»ÆµŖµČĘųĢ壻·Ū³¾Ö÷ŅŖÖøŅ»Š©¹ĢĢ劔æÅĮ££®PM2.5×÷ĪŖ½Ģ²ÄŠĀŅżČėµÄÄŚČŻÓ¦ŅżĘšĶ¬Ń§ĆĒµÄÖŲŹÓ£¬PM2.5ÓÖ³ĘæÉČė·ĪæÅĮ££¬ĘäæÅĮ£“óŠ”Ō¶Ō¶“óÓŚĪ¢¹ŪµÄ·Ö×Ó£¬Ę䥓Ō“Ö÷ŅŖÓŠÉś»īÖŠµÄ²»ŗĻĄķ·ŁÉÕŅŌ¼°Ęū³µĪ²Ęų”¢¹¤ŅµŃĢ³¾µČ£¬PM2.5ŹĒŌģ³É»Ņö²ĢģĘųµÄÖ÷Ņņ£®»īŠŌĢæ¾ßÓŠĪüø½ŠŌ£¬ÄÜĪüø½Ņ»Š©Č¼ĮĻ”¢ÓŠŗ¦ĘųĢåŗĶŅģĪ¶µČ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗ¢Ł¼Ó“ó²śŅµ½į¹¹µ÷Õū£¬¼ÓæģĢŌĢĀäŗó²śÄܶŌPM2.5µÄÖĪĄķÄÜĘšµ½»ż¼«×÷ÓĆ£» ¢Ś¼ÓĒæ½ØÖž¹¤µŲ”¢µĄĀ·Ńļ³¾æŲÖʶŌPM2.5µÄÖĪĄķÄÜĘšµ½»ż¼«×÷ÓĆ£»¢Ū·¢Õ¹³ĒŹŠ¹«¹²½»ĶØ£¬Ģį³«Ź¹ÓĆĒå½ąÄÜŌ“¶ŌPM2.5µÄÖĪĄķÄÜĘšµ½»ż¼«×÷ÓĆ£» ¢ÜŃĻĄ÷²é“¦·ŁÉÕĄ¬»ų”¢½ÕøѶŌPM2.5µÄÖĪĄķÄÜĘšµ½»ż¼«×÷ÓĆ£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĮĖæÕĘųµÄĪŪČ¾¼°ĘäĪ£ŗ¦£¬×¢Ņā»·±£ĪŹĢāŅŃ¾ŅżĘšĮĖČ«ĒņµÄÖŲŹÓ£¬Ļ°Ģā»ł“”ŠŌ±Č½ĻĒ棬Ö÷ŅŖ³öĻÖŌŚŃ”ŌńĢāŗĶĢīæÕĢāÖŠ£®


 Õć“óÓÅѧŠ”ѧğ¼¶ĻĪ½Ó½Ż¾¶Õć½“óѧ³ö°ęÉēĻµĮŠ“š°ø
Õć“óÓÅѧŠ”ѧğ¼¶ĻĪ½Ó½Ż¾¶Õć½“óѧ³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+--ÄĘŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+1¼Ū | B£® | 2H--1øöĒā·Ö×ÓÓÉ2øöĒāŌ×Ó¹¹³É | ||
| C£® | 2H2O--2øöĖ®·Ö×Ó | D£® | $\stackrel{+3}{Al}$--1øöĀĮĄė×Ó“ų3øöµ„Ī»ÕżµēŗÉ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĪŖŹ¹·¢ĆęŹ³Ę·ĖÉČķæÉæŚ£¬ÖĘ×÷Ź±æÉĢķ¼ÓŹŹĮæĢ¼ĖįĒāÄĘ | |
| B£® | °×É«ĪļÖŹŌģ³ÉµÄĪŪČ¾³ĘĪŖ°×É«ĪŪČ¾ | |
| C£® | Ć¹±äŗģŹķ”¢»ØÉśÕōÖóŗó»¹æɼĢŠųŹ³ÓĆ | |
| D£® | ÓŠ»śĪļ¶¼ŹĒŗ¬Ģ¼µÄ»ÆŗĻĪļ£¬ŅŅ“¼”¢Ģ¼ĖįøĘŅ²ŹĒÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
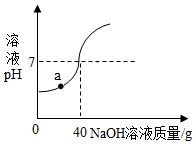 ÖŠŗĶ·“Ó¦ŌŚ¹¤Å©ŅµÉś²śÖŠÓ¦ÓĆ¹ć·ŗ£®ĻÖ½«ČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĒāŃõ»ÆÄĘČÜŅŗµĪ¼Óµ½60gĻ”ĮņĖįÖŠ£¬²āµĆČÜŅŗpHÓė¼ÓČėµÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£®
ÖŠŗĶ·“Ó¦ŌŚ¹¤Å©ŅµÉś²śÖŠÓ¦ÓĆ¹ć·ŗ£®ĻÖ½«ČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĒāŃõ»ÆÄĘČÜŅŗµĪ¼Óµ½60gĻ”ĮņĖįÖŠ£¬²āµĆČÜŅŗpHÓė¼ÓČėµÄĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
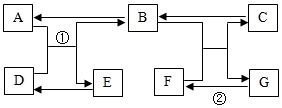 A”«GŹĒ³õÖŠĖłŃ§µÄ³£¼ūĪļÖŹ£¬Ęä×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦ĪļŗĶÉś³ÉĪļ”¢·“Ó¦Ģõ¼žŅŃĀŌČ„£©£¬A”¢B³£ĪĀĻĀĪŖĪŽÉ«ĘųĢåĒŅ×é³ÉŌŖĖŲĻąĶ¬£¬CŹĒ“óĄķŹÆµÄÖ÷ŅŖ³É·Ö£¬DĪŖŗŚÉ«¹ĢĢåEĪŖŗģÉ«¹ĢĢ壮Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
A”«GŹĒ³õÖŠĖłŃ§µÄ³£¼ūĪļÖŹ£¬Ęä×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦ĪļŗĶÉś³ÉĪļ”¢·“Ó¦Ģõ¼žŅŃĀŌČ„£©£¬A”¢B³£ĪĀĻĀĪŖĪŽÉ«ĘųĢåĒŅ×é³ÉŌŖĖŲĻąĶ¬£¬CŹĒ“óĄķŹÆµÄÖ÷ŅŖ³É·Ö£¬DĪŖŗŚÉ«¹ĢĢåEĪŖŗģÉ«¹ĢĢ壮Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÉśĆüµÄŌŠÓżÓėĪ¬ĻµŠčŅŖĖ® | B£® | .Ė®ÓŠ¹ĢĢ唢ŅŗĢ唢ĘųĢåČżÖÖדĢ¬ | ||
| C£® | .µē½āĖ®Éś³ÉĒāĘųŗĶŃõĘų | D£® | .Ė®ŹĒÓÉ·Ö×Ó¹¹³ÉµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
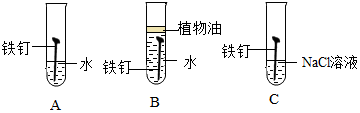
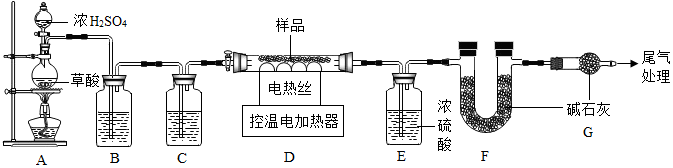
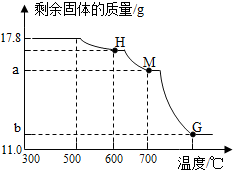
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com