
����Ŀ��2018��10��28�գ�����Ϊ֮�����ĵ�һ��001A������ĸ�����κ��ԣ���־���ҹ��ں�������������ȡ���ش�ͻ�ơ���������ѧ֪ʶ��գ�
��1���Ͻ��Ǻ�ĸ��������ϣ������Ͻ��������ᡢӲ�ȴ�ǿ�Ŀ���ʴ�����ں�ĸ�����б��������������£������к�ǿ����ʴ�Ե�ԭ����_____��
��2����ĸ�������Ϳ�ϸ�����Ϊ�˷�ֹ����������_____�Ӵ������⡣
��3�����캽ĸ�õ��ѺϽ𡣹�ҵ���ѹ�������һ����Ӧ�Ļ�ѧ����ʽΪTiF4+2H2SO4![]() 4HF+2X+TiO2����X�Ļ�ѧʽΪ_____��
4HF+2X+TiO2����X�Ļ�ѧʽΪ_____��
���𰸡�ͨ������£����ܺͿ����е�������Ӧ�������ܵ�����������Ĥ ˮ������ SO3
��������
��1�������£��������ڿ����в����ױ���ʴ��ԭ���ǣ�ͨ������£����ܺͿ����е�������Ӧ�������ܵ�����������Ĥ�����ͨ������£����ܺͿ����е�������Ӧ�������ܵ�����������Ĥ��
��2����ĸ�������Ϳ�ϸ�����Ϊ�˷�ֹ����������ˮ�������Ӵ������⡣���ˮ��������
��3����TiF4+2H2SO4![]() 4HF+2X+TiO2��֪����Ӧǰ����ԭ�Ӷ���1������ԭ�Ӷ���4������ԭ�Ӷ���4������Ӧǰ��ԭ����2������Ӧ��Ӧ����2����������2X�У���Ӧǰ��ԭ����8������Ӧ��Ӧ����8��������6��������2X�У����X�Ļ�ѧʽΪSO3��
4HF+2X+TiO2��֪����Ӧǰ����ԭ�Ӷ���1������ԭ�Ӷ���4������ԭ�Ӷ���4������Ӧǰ��ԭ����2������Ӧ��Ӧ����2����������2X�У���Ӧǰ��ԭ����8������Ӧ��Ӧ����8��������6��������2X�У����X�Ļ�ѧʽΪSO3��
���SO3��


 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����5�֣�A��B��C��D��EΪ���л�ѧ�������������ʣ�����֮�������ͼ��ʾ�Ĺ�ϵ����������ʾ���ʾ�һ����Ӧ��ת��Ϊ��һ�����ʣ���������ʾ�����������ܷ�����ѧ��Ӧ�����ַ�Ӧ������P��Ӧ��������ȥ������ش��������⣺
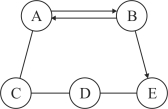
��1����A��BΪ���Ԫ����ͬ�����壬EΪ����ʯ����Ҫ�ɷ֣���B�Ļ�ѧʽΪ ����
��D�����Ϊ ������������������������������������������
��2����A���ܹ���������������壬B��һ����õ��ܼ���D��ˮ��Һ����ɫ��
��C��D��Ӧ�Ļ��������� ��
D��E��Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȷд����ѧ���
��1��������ԭ��___��
��2��������___��
��3��д���Ȼ����Ļ�ѧʽ�������Ԫ�صĻ��ϼ�___��
��4����ˮ���ɵķֽⷴӦ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬѧ����ʵ���Ҵ�ŵ�һƿ�������ƹ���������Һ������к�ʵ�顣
(1)��֪��ˮ���ܶ�Ϊ1.0g/mL��ʵ��������100g������������Ϊ5%������������Һ����Ҫ��ȡ��������5g����Ҫ��ȡˮ________mL����ȡʱ�IJ�������ͼ��ʾ���ò�������������Һ��������������Ӱ����________________��

(2)���������Ƶ�����������Һ���кͷ�Ӧʵ�飬���������ݲ��������������ж��������Ʊ����ˡ����û�ѧ����ʽ˵���������Ʊ��ʡ��μ�����������ݵ�ԭ��______________��
(3)Ϊ̽�����������Ƿ���ȫ���ʣ��������������ʵ�鷽����
����1��ȡ������������������Һ��Ʒ���μӼ��η�̪��Һ����Һ��ɺ�ɫ
����2��ȡ������������������Һ��Ʒ�����뱥��ʯ��ˮ�����ã�ȡ�ϲ���Һ���μӼ��η�̪��Һ�������ܺ�ɫ��
����������Ϊ��Ʒ�л������������ƣ�û����ȫ������
�ٿ�����Ϊ����������ʵ�鷽�������ܴﵽĿ�ģ�����������_________________��
���������һ����������֤���������Ƿ���ȫ���ʡ�_____________________
(4)����������2�����˶�����������������������ƹ���ı��ʳ̶ȡ�ȡ10g��Ʒ����90gˮ�У������еμӹ�������ʯ��ˮ���Գ�������ϴ�ӡ���ɺ����Ϊ0.5g������Ʒ���������Ƶ�����������_____________?
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ����Ҫ�����ʣ���ʵ�����г������ܽ����ʡ�������Һ��
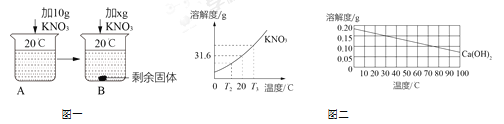
��1����50gˮ���ܽ�һ����KNO3����IJ������£��������ͼһʵ�������ܽ�����ش𣺵�x=__________gʱ��B��ǡ��û�й���ʣ�ࣻ
��2��ijͬѧ��һƿ�������������ƹ��壨�ܽ��������ͼ����ʾ����Ʒ��ȡ��0.2g�����뵽30��ʱ100gˮ�У�����ܽ����ˣ��Ƶ�ʣ�����0.08g�������жϣ���ҺΪ__________��ѡ��������������������������
��3����������л����������������ƣ����Բ�ȡ__________�ķ����ᴿ����أ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ᡢ����Ǽ�����Ҫ�Ļ����
��1����ʢ��Ũ�����Ũ������Լ�ƿ�ǣ��������ܰ��������ֿ�����ԭ����_____��
��2��100 g��������Ϊ10%��ϡ�����100 g��������Ϊ10%������������Һ��ַ�Ӧ����Һ��pH_____7��������������С������������������
��3����������ʵ��װ�����ľ����У�ij��ѧ��ȤС���ͬѧ�������ͼ��ʾ��װ�á�
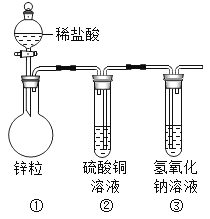
��д��װ�ü��з�����Ӧ�Ļ�ѧ����ʽ_____��
�ڱ�װ���л����ʲô����_____��
��4��ijͬѧΪ�˳�ȥNaCl��Һ��CaCl2��MgCl2��Na2SO4������ȡ���Σ�����������ͼ��ʾ��[��ʾ��Mg(OH)2��BaSO4��BaCO3������ˮ]
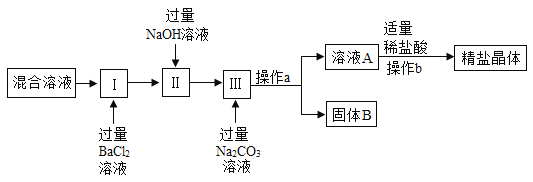
��д����I���м������BaCl2��Һ��������Ӧ�Ļ�ѧ����ʽ_____��
�ڲ���a������Ϊ_____��
��ͨ������a������ҺA�г��Ȼ����⣬�����е���������Щ_____��
��5����20 g�����Ȼ������ʵ�̼���ƹ����м���100 gϡ���ᣬǡ����ȫ��Ӧ���õ�115.6g��������Һ��������ϡ�����������������_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ����ˮ���̵���Ҫ����������ͼ��
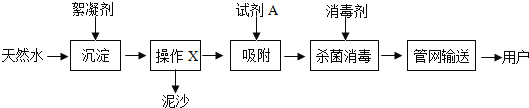
���ϣ����õ�������������[KAl(SO4)12H2O]����������Һ��(Cl2)
�ش��������⣺
(1)����X��������____���Լ�A��������____��
(2)����������������Ϊ��ˮ��Ӧ��������������״����������Ļ�ѧʽΪ____��Һ����ˮ�����ʷ�Ӧ����һЩ�������к������ʣ��������ȼ���(CHCl3)�����ȼ�������____(�����л���������������)
(3)�������(K2FeO4)����������������������ɱ��ʱ����������������״������������Ԫ�صĻ��ϼ���____��
(4)����ˮ���ľ�ˮ����____(������������������)��Ӳˮ��������ˮ�������н�Ӳˮ�����ķ�����____�������˷���ˮ�еIJ���Ca2+��Mg2+ת��Ϊ��������ͨ����˵��ˮ����ˮ������Ҫ�ɷ�Ϊ____��
(5)����ˮ��ͨ��������Cl����������ˮ���еμ�����ϡ�����____���飬������____����˵��ˮ�к���Cl����
(6)ʵ����������ˮ��ȡ����ˮ��������ƿ�ͨ��Ҫ���뼸����ʯ�����Ƭ��������____
(7)�����������ϡ��Һ����ˮ��ԭ�����ɱ�ʾΪ��2H2O![]() 2H2��+O2�������һ��������������ϡ��Һ�Ĺ����У�����˵����ȷ����_____
2H2��+O2�������һ��������������ϡ��Һ�Ĺ����У�����˵����ȷ����_____
A ��Һ����Ԫ��������� B ��Һ���⡢��Ԫ�������Ȳ���
C ��Һ����Ԫ������������С D ��Һ��pH��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����˫��������һ�ֳ�����װʳƷ�ı��ʼ��������տ����е�������������̼��ˮ�����ȡ���ѧ��ȤС���ͬѧ��ijʳƷ���з���һ����˫�����������ǩ��ͼ��ʾ��ͬѧ�Ƕ�������õ���˫������������Ʒ�ܺ��棬���ʵ�����̽����

��������⣩������˫����������ijɷ���ʲô��
���������ϣ�
�����Ȼ�����Һ�ڳ����·�����Ӧ�����Ȼ�������Fe+2FeCl3�T3FeCl2��
���������룩���ù�����һ���л���̿���ܺ��м�________________��
��ʵ��̽�����±���С��ͬѧ��Ƶ�ʵ�鷽���ͼ�¼��ʵ�鱨�棬���㲹��������
ʵ����� | ʵ������ | ʵ����� |
��ȡ3g������Ʒ��ϸ�۲죬�ô��������壬�����ձ��У���20 mLˮ�����¶ȼƲ����ܽ�ǰ��Һ���¶ȣ����ˣ�������Һ���á� | ������Ʒ���к�ɫ��ĩ�� �϶��ɫ���弰��������ɫ���壬������ɫ��ĩ���Ա��� ���������¶ȼ��¶������Ա仯���õ���ɫ��Һ | ��Ʒ��____________ |
��ȡ����������ɫ��Һ���μ���ɫ��̪�� | ��Һ����ɫ��Ϊ��ɫ | ��Ʒ��һ����Ca(OH)2 |
��ȡ����������Ʒ�����Թ� �У����������Լ�Y���ô����ܵĵ�����Ƥ�������Թܿڣ�������һ���������ʯ��ˮ�С� | �Թ��й������٣��д�����ɫ����������õ�dz��ɫ��Һ����������ɫ���岻�ܣ������ʯ��ˮ����ǡ� | ��Ʒ�к��л���̿��CaCO3 |
��ʵ�����ɣ�ȷ���˾�����˫����������ijɷֺ�λͬѧ��������������⣺
��������м����Լ� Y ����Һȴ���ʻ�ɫ��ԭ����_______________��
���������ϵ�֪��������������ʱ��Ϊ�˴ﵽ���õ�����Ч�����������м����������Ȼ��ơ������ʵ��˵���Ȼ��ƴ���ʱ��������Ч�����ã�__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�����ʾ��ȷ����
A.��������FeOB.������ԭ�ӣ�O3
C.�����ӣ�Ca+2D.������ ![]()
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com