
| A. | 反应条件不同 | B. | 生成物都是单质 | ||
| C. | 都遵循了质量守恒定律 | D. | 两个反应都属于分解反应 |
分析 A、水通电分解和过氧化氢分解的条件,进行分析判断.
B、通电分解生成氢气和氧气,过氧化氢分解生成水和氧气,进行分析判断.
C、根据一切化学反应均遵守质量守恒定律,进行分析判断.
D、分解反应:一种物质反应后生成两种或两种以上的物质,其特点可总结为“一变多”.
解答 解:A、水通电分解和过氧化氢分解的条件分别是通电、常温下就能反应,反应条件不同,故选项说法正确.
B、通电分解生成氢气和氧气,过氧化氢分解生成水和氧气,生成的水是化合物,故选项说法错误.
C、一切化学反应均遵守质量守恒定律,故选项说法正确.
D、两个反应均符合“一变多”的特征,均属于分解反应,故选项说法正确.
故选:B.
点评 本题难度不大,掌握电解水与过氧化氢分解的反应原理、质量守恒定律、分解反应的特征等是正确解答本题的关键.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:初中化学 来源: 题型:实验探究题
| 实验一 | 实验二 |
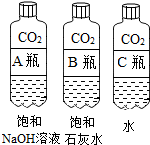 | 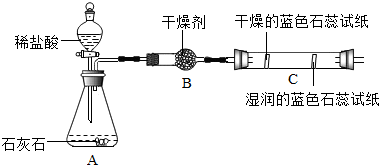 |
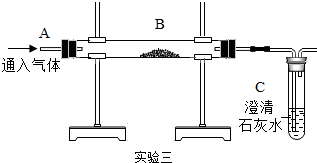
| 实验四 | |
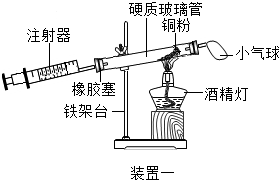 | 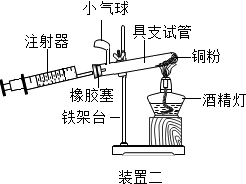 |
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 30mL | 20mL | 12mL | 16% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
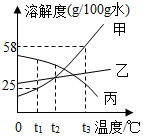 如图为甲、乙、丙三种固体物质的溶解度曲线,请据图回答:
如图为甲、乙、丙三种固体物质的溶解度曲线,请据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
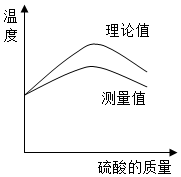 实验小组欲利用氢氧化钠溶液与硫酸反应探究中和反应过程中的热量变化.请你参与探究实验.
实验小组欲利用氢氧化钠溶液与硫酸反应探究中和反应过程中的热量变化.请你参与探究实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
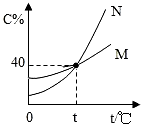 如图为M、N 两种固体饱和溶液溶质的质量分数(C%)随温度(t)变化的曲线.
如图为M、N 两种固体饱和溶液溶质的质量分数(C%)随温度(t)变化的曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
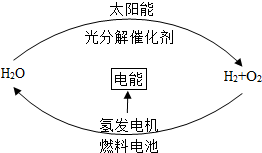 目前,科学家提出了一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法正确的是( )
目前,科学家提出了一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法正确的是( )| A. | 燃料电池能够使化学反应产生的能量转化为电能 | |
| B. | 在此循环中发生了反应:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | |
| C. | 该氢能源的循环体系能够实现电能和太阳能的相互转化 | |
| D. | 目前未能使用氢气作为普通燃料的主要原因是氢气易爆炸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com