
质量为50g溶质质量分数为20%的氢氧化钾溶液和质量为50g溶质质量分数为20%的稀硫酸混合,所得溶液的PH( )
|
| A. | 小于7 | B. | 等于7 | C. | 大于7 | D. | 不确定 |
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:初中化学 来源: 题型:
下列有关水的说法中错误的是()
A. 自然界中的河水、井水和湖水都属于混合物
B. 实验室电解水时,正极端玻璃管内的气体是氢气
C. 农业上合理使用化肥和农药有利于水资源的保护
D. 生活中可以通过煮沸降低水的硬度
查看答案和解析>>
科目:初中化学 来源: 题型:
在某无色溶液中,能大量共存的是( )
|
| A. | Na+,Fe2+,NO3﹣,Cl﹣ | B. | Na+,K+,NO3﹣,CO32﹣ |
|
| C. | Ba2+,K+,SO42﹣,Cl﹣ | D. | NH4+,K+,OH﹣,SO42﹣ |
查看答案和解析>>
科目:初中化学 来源: 题型:
下列离子在水溶液中无色且能大量共存的一组是( )
|
| A. | Ca2+,K+,Cl﹣,NO |
|
| B. | Na+,Cu2+,NO |
|
| C. | Fe3+,Na+,OH﹣,NO |
|
| D. | K+,H+,SO |
查看答案和解析>>
科目:初中化学 来源: 题型:
下列没有运用中和反应原理的是( )
|
| A. | 服用含氢氧化镁的药物,可以治疗胃酸过多症 |
|
| B. | 用熟石灰改良酸性土壤 |
|
| C. | 蚊虫叮咬处涂上肥皂水,可减轻痛痒 |
|
| D. | 用生石灰做干燥剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:
将0.4%的氢氧化钠溶液滴加到2mL0.4%的盐酸中,测得混合液的pH变化曲线如图.某学习小组对加入0~VmL氢氧化钠过程中,所得混合液pH增大原因进行了如下探究:
【猜想假设】
猜想Ⅰ:pH增大是因为 ;
猜想Ⅱ:pH增大是因为发生了反应,写出反应方程式 .
【实验探究】
为验证猜想Ⅱ,请你帮助该小组完成下列实验.(可供选择的实验用品有:pH计、0.4%的氢氧化钠溶液、0.4%的盐酸、水.)
(1)向2mL0.4%的盐酸中加入VmL0.4%的氢氧化钠溶液,用pH计测得混合液的pH=7.
(2)向2mL0.4%的盐酸中加入VmL ,用pH计测得混合液的pH 7(填“>”、“=”或“<”).
综合(1)和(2)证明猜想Ⅱ成立.
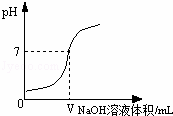
查看答案和解析>>
科目:初中化学 来源: 题型:
镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的.主要步骤如下:
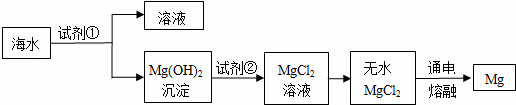
(1)上述步骤中试剂①应过量,理由是 .
(2)请写出Mg(OH)2沉淀与试剂②发生中和反应的化学方程式 .
(3)无水MgCl2在熔融状态下通电得到金属镁和物质A,氢气在物质A中燃烧生成物质B,则物质A和B的化学式分别为:A ,B .
查看答案和解析>>
科目:初中化学 来源: 题型:
用实验探究铝和铜的金属活动性强弱,若提供的试剂只有:氯化铜溶液、氯化铝溶液、铝、铜和稀盐酸,对此下列说法正确的是()
A.最多只能设计一种实验方案
B.氯化铜溶液是不可或缺的试剂
C.选用两种合适的试剂即可实现实验目的
氯化铝溶液中加入铜不能探究金属活动性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com