
| A. | 苹果汁:3.1 | B. | 玉米粥:7.5 | C. | 牛奶:6.5 | D. | 番茄汁:4.2 |
科目:初中化学 来源: 题型:解答题
 某饮用水标签上的部分文字如图,请回答:
某饮用水标签上的部分文字如图,请回答: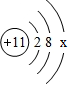 ,其中x=1.
,其中x=1.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 点燃混合气体 | B. | 把混合气体通入足量的水 | ||
| C. | 把混合气体通入足量的澄清石灰水 | D. | 把混合气体通过足量的灼热氧化铜 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )
2016年“世界环境日”中国确定的主题为“改善环境质量,推动绿色发展”.下列做法与之相违背的是( )| A. | 提倡绿色出行,发展公共交通 | B. | 积极植树、造林、种草 | ||
| C. | 农作物的秸杆就地焚烧 | D. | 工业废水处理达标后排放 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用熟石灰改良酸性土壤 | |
| B. | 用氢氧化铝治疗胃酸过多 | |
| C. | 用生石灰做干燥剂 | |
| D. | 印染厂的废水中含有少量氢氧化钠,可加入适量的稀硫酸除去 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
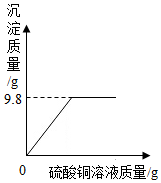 向一定量的氢氧化钠溶液中逐渐加入硫酸铜溶液,生成硫酸钠和氢氧化铜沉淀,测得生成沉淀的质量与所加硫酸铜溶液的质量关系如图所示.
向一定量的氢氧化钠溶液中逐渐加入硫酸铜溶液,生成硫酸钠和氢氧化铜沉淀,测得生成沉淀的质量与所加硫酸铜溶液的质量关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 组别 | 样品质量 | CO2体积 |
| 第1组 | 0.20g | 22.3mL |
| 第2组 | 0.20g | 22.4mL |
| 第3组 | 0.20g | 22.5mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com