
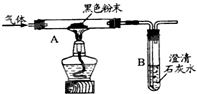
 我校兴趣小组几位同学,在学习了九年级化学第六单元后,对能产生二氧化碳的一些物质产生了兴趣.其中几位同学对实验室的草酸[C2H2O4]产生了兴趣,她们请教老师得知:草酸的化学性质与碳酸相似.碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.他们对此展开了探究:
我校兴趣小组几位同学,在学习了九年级化学第六单元后,对能产生二氧化碳的一些物质产生了兴趣.其中几位同学对实验室的草酸[C2H2O4]产生了兴趣,她们请教老师得知:草酸的化学性质与碳酸相似.碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.他们对此展开了探究:| 实 验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.54 | 3.08 | 4.4 | m |
分析 (1)根据质量守恒定律进行分析;
(2)根据二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水进行分析;
根据一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳进行分析;
(3)根据二氧化碳不具有还原性,只要是黑色粉末变成红色,就说明存在还原性物质,能说明存在一氧化碳,特别是在验证一氧化碳时,注意尾气处理,否则没反应的一氧化碳会污染空气进行分析.
(4)碳酸钙的质量分数可根据第1次或第2次实验中二氧化碳的质量求出.根据化学方程式得出各物质之间的质量比,列出比例式,即可求出参加反应的CaCO3的质量,然后再根据质量分数公式进行计算即可.
解答 解:(1)在化学反应前后,元素的种类不变,所以根据草酸中含有氢、氧元素,可推测生成物中含有水;
(2)二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,所以将生成的气体通入澄清的石灰水,实验现象是:澄清石灰水变浑浊,判断生成物中含有二氧化碳;反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
一氧化碳具有还原性,能将黑色的氧化铜还原为红色的铜,所以本题答案为:CuO;
(3)二氧化碳不具有还原性,只要是红色粉末变成黑色,就说明存在还原性物质,能说明存在一氧化碳,特别是在验证一氧化碳时,注意尾气处理,否则没反应的一氧化碳会污染空气.
(4)①为避免样品中碳酸钙不能完成反应,可把样品粉碎,增大样品与盐酸的接触面积,此举还可以加快反应的速率;
故答案为:增大石灰石与盐酸的接触面积,加快反应速率.
②因为第3次反应已是完全反应,不再有气体产生,故第四次反应生成的气体质量的第三次的一样多,即m=4.4.
③设第1次实验中样品中的碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 1.54g
$\frac{100}{44}=\frac{x}{1.54g}$,解之得:x=3.5g,
石灰石中碳酸钙的质量分数为:$\frac{3.5g}{5g}$×100%=70%.
答:石灰石中碳酸钙的质量分数为80%.
故答案为:
(1)氢和氧;
(2)澄清石灰水变浑浊,CO2+Ca(OH)2═CaCO3↓+H2O.CuO;
(3)支持,只要根据氧化铜由黑色变为红色,就可判断三种氧化物中一定含有一氧化碳;没有尾气的处理装置,添加酒精灯在装置最后.
(4)增大石灰石与盐酸的接触面积,加快反应速率;4.4;70%
点评 验证二氧化碳将气体通过澄清石灰水,验证一氧化碳时将气体通过金属氧化物,看是否能还原出金属,要注意有尾气处理装置.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 红磷在空气中燃烧,产生大量白雾 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色的四氧化三铁 | |
| D. | 向氢氧化钠溶液中滴入氯化铁溶液,产生红褐色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
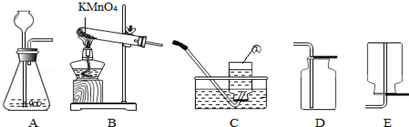
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
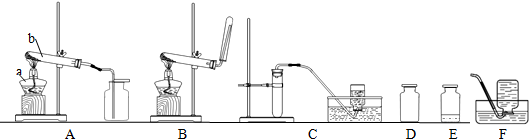
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选顼 | 物质 | 杂质(少量) | 试剂或方法 |
| A | H20 | 色素 | 活性炭 |
| B | Mn02 | KCl | 溶解、过滤、洗涤、烘干 |
| C | N2 | 02 | 通过红热的木炭 |
| D | C02 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | CO2气体 | CO气体 | 通入氧气,点燃 |
| B | NaCl溶液 | Na2CO3溶液 | 滴入适量稀盐酸至无气泡产生 |
| C | Fe粉 | CuO粉 | 加入足量稀盐酸充分反应后过滤 |
| D | Cu(NO3)2溶液 | AgNO3溶液 | 加足量铜粉充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com