
| 编号 | 实验事实 | 实验结论 |
| A | 某溶液使酚酞溶液变红 | 该溶液一定是NaOH溶液 |
| B | 某物质中含有一种元素 | 该物质一定是单质 |
| C | 常温下,测定某溶液的PH=3 | 该溶液一定呈酸性 |
| D | 某气体不能使带火星的木条复燃 | 该气体一定不含氧气 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、依据显碱性的溶液能使酚酞试液变红色分析解答;
B、依据单质的概念分析解答即可;
C、依据当溶液的pH小于7时,溶液显酸性分析解答;
D、依据空气中含有氧气,但空气不能使带火星的木条复燃进行判断即可.
解答 解:A、能使酚酞试液变红的溶液呈碱性,但是不一定是氢氧化钠溶液,比如氢氧化钙溶液、碳酸钠溶液,错误.故选项错误;
B、单质是含有一种元素的纯净物,所以只含一种元素不一定是单质,如氧气与臭氧的混合物,故此选项错误;
C、当溶液的pH小于7时,溶液显酸性.故选项正确;
D、含有氧气的气体不一定能使带火星的木条复燃,例如空气中含有氧气,空气不能使带火星的木条复燃.故选项错误.
故选C.
点评 解答本题要充分理解各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 如图是初中化学中常见化合物间的转化关系,其中A在常温下是液体,F是人体胃液中助消化的酸,A和B在不同的条件下会发生不同的化学反应.(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.)
如图是初中化学中常见化合物间的转化关系,其中A在常温下是液体,F是人体胃液中助消化的酸,A和B在不同的条件下会发生不同的化学反应.(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.)查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
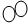 ”和“
”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如下图所示,下列说法正确的是( )
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如下图所示,下列说法正确的是( )
| A. | 参加反应的“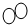 ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| B. | 该反应是化合反应 | |
| C. | 该反应有2种生成物 | |
| D. | 每个生成物分子由3个原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com