
分析 (1)除去硫酸镁用氢氧化钡,除去氯化钙用碳酸钠,碳酸钠还可以除去过量的氢氧化钡,所以先加氢氧化钡,再加碳酸钠,过滤除去沉淀和泥沙,再加入稀盐酸除去过量的碳酸钠,再蒸发可得到氯化钠;(2)精盐水变为铵盐水,缺少氮元素,所以气体是氨气;分解反应是碳酸氢钠加热得到碳酸钠、水和二氧化碳;(3)①氯化钠的溶解度随温度变化不大,所以用蒸发溶剂的方法;②根据t1℃时,碳酸钠的溶解度考虑.
解答 解:(1)除去硫酸镁用氢氧化钡,除去氯化钙用碳酸钠,碳酸钠还可以除去过量的氢氧化钡,所以先加氢氧化钡,再加碳酸钠,过滤除去沉淀和泥沙,再加入稀盐酸除去过量的碳酸钠,再蒸发可得到氯化钠,所以正确的操作顺序是④②①③⑤;
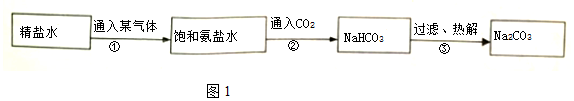
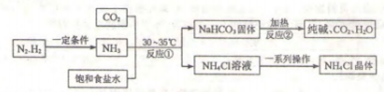
(2)精盐水变为铵盐水,缺少氮元素,所以气体是氨气;分解反应是碳酸氢钠加热得到碳酸钠、水和二氧化碳,所以方程式是:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
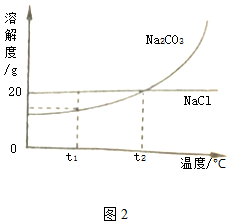
(3)①氯化钠的溶解度随温度变化不大,所以用蒸发溶剂的方法;②根据t2℃时,碳酸钠的溶解度是20g,所以100g水中最多溶解20g碳酸钠,所以25g水中最多溶解5g碳酸钠.
故答案为:(1)④②①③⑤(2)NH3; 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;(3)①蒸发结晶;②25.
点评 解答本题关键是熟悉溶解度曲线表示的意义,知道溶解度的四要素.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 操作步骤 | 判断依据 | 对应结论 |
| 把适量固体置于试管中,加入足量水溶解,再加入足量氯化钙溶液,静置后滴加酚酞试液 | 不产生沉淀,溶液变红色,或产生白色沉淀,溶液变红色,或产生白色沉淀,溶液不变色 | 氢氧化钠没有变质,或氢氧化钠部分变质,或氢氧化钠全部变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③④ | B. | 只有①③④ | C. | 只有① | D. | 只有①④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - | |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.5 | 77.3 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气、氮气、空气 | B. | 氧气、空气、氮气 | C. | 空气、氮气、氧气 | D. | 氮气、空气、氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该反应是置换反应 | |
| B. | 若X是Al,R是Ag,则反应后溶液质量减少 | |
| C. | X的金属活动性比R强 | |
| D. | X可能是Fe,R可能是Cu |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com