
| 实验操作 | 实验现象 | 实验结论 |
| 取甲同学的生成物,过滤,向滤渣中加入稀盐酸 | 白色沉淀溶解,产生无色无味的气体 | 该溶液不是硫酸钠溶液,而是碳酸钠溶液 |

| 实验操作 | 实验现象 | 结论 |
| 向反应后的溶液中继续加入盐酸 | 立即产生大量气泡 | 猜想三正确 |
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:初中化学 来源: 题型:选择题
| 选项 | 目的 | 方法 |
| A | 除去氯化铁中的盐酸 | 加入适量的铁粉 |
| B | 除去NaCl溶液中的CaCl2 | 加入适量的Na2CO3溶液,过滤 |
| C | 除去HCl气体中的CO2 | 通过足量的NaOH溶液 |
| D | 除去炭粉中的铁粉 | 加入足量的CuSO4溶液后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用洗洁精的乳化作用洗去餐具上的油污 | |
| B. | 为了防止食品变质腐烂,我们可以用甲醛溶液来浸泡食品 | |
| C. | 食盐中加入适量的碘可预防甲状腺肿大 | |
| D. | 用灼烧法鉴别蚕丝和涤纶面料 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
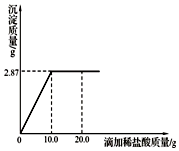 为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.(计算结果均保留1位小数)
为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.(计算结果均保留1位小数)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 污水净化过程中,要经过测pH、沉降、过滤、吸附、消毒等步骤 | |
| B. | 无色无味的废液都是无毒无害的,可以直接排放 | |
| C. | 排放的废水中氮、磷含量过高会导致“水华”和“赤潮”现象 | |
| D. | 经过净化的污水可以利用太阳能分解获得氢能 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ①向所得沉淀A中加入过量稀盐酸,充分反应: | 出现白色沉淀B 和蓝色溶液,没有气泡产生 | 自色沉淀B是BaSO4(或硫酸钡) |
| ②取少量无色滤液M于试管中,滴入酚酞溶液; | 溶液不变色 | 则滤液M 中一定含有的溶质是NaCl(或氯化钠) |
| ③取步骤②中溶液,加入适量Na2SO4溶液,充分反应: | 无明显现象 | |
| ④另取少量无色滤液M于试管中,加入几粒锌粒; | 无明显现象(或锌粒表面无红色固体生成、无气体放出) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 均一、稳定的液体一定是溶液 | |
| B. | 溶液一定是无色透明的 | |
| C. | 食盐水能导电是因为食盐水中含有较多自由移动的离子 | |
| D. | 硝酸铵溶于水后溶液温度升高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com