
科目:初中化学 来源: 题型:选择题

| A. | 图1中甲溶液一定是饱和溶液 | |
| B. | 图2中甲溶液一定是不饱和溶液 | |
| C. | 图3中N表示的是乙的溶解度曲线 | |
| D. | 图2中两溶液降温至30℃都会析出晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭在氧气中燃烧生成黑色固体 | |
| B. | 硫在空气中燃烧产生明亮的蓝紫色火焰,生成无色有刺激性气味的气体 | |
| C. | 镁条在空气中燃烧,发出耀眼的白光,生成白色固体 | |
| D. | 铁片放入稀硫酸中,铁片表面有气泡产生,溶液由无色逐渐变黄色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
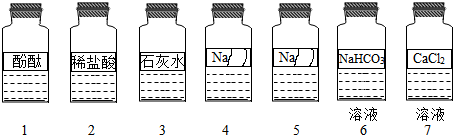
| 实验操作 | 实验现象 | 实验结论 |
实验1 | 溶液均由无色变成红色 | 4、5号溶液均不可能是上述猜想中的NaCl溶液. |
实验2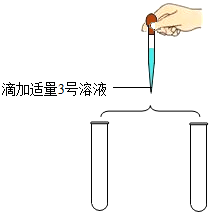 | 均产生白色沉淀 | 4、5号溶液可能分别是Na2SO3溶液和Na2CO3溶液中的一种.写出其中一个反应的化学方程式:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,或Na2SO3+Ca(OH)2═CaSO3↓+2NaOH |
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量4号溶液于试管中,加入足量CaCl2溶液 ②过滤,向滤液中滴加几滴酚酞试液 | ①有白色沉淀生成 ②酚酞试液变红色 | 4号溶液是部分变质的NaOH溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 金刚石可做钻石,是因为金刚石硬度很大 | |
| B. | 一氧化碳有毒,是因为一氧化碳与血红蛋白结合,使血红蛋白不能很好地与氧气结合 | |
| C. | 干冰可用于人工降雨,是因为干冰发生了化学变化 | |
| D. | 金刚石、石墨、C60都是有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有机物一定含有碳元素,所以含碳元素的化合物一定是有机物 | |
| B. | 置换反应中有单质生成,所以有单质生成的反应一定属于置换反应 | |
| C. | 含碳元素的物质在O2中充分燃烧会生成CO2,所以在O2中燃烧能生成CO2的物质一定含碳元素 | |
| D. | 盐的组成中含有金属阳离子与酸根离子,所以盐中一定不含氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 先用清水润湿头发 | |
| B. | 向头发上涂洗发剂揉搓 | |
| C. | 用清水冲洗头发 | |
| D. | 向头发上涂护发素揉搓,再用清水冲洗干净 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
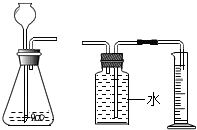 为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:| 实验步骤 | 现象 | 结论 |
| ①将足量铁粉与锌粉分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率: Fe>Zn | 反应速率与反应物的金属的活动性强弱有关 |
| ②将等质量锌粉与锌片分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率: 锌粉>锌片 | 反应速率与反应物的接触面积大小有关 |
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积 | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com