
��8�֣�ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ����ʾ����֪��BaCl2��Na2CO3��BaCO3����2NaCl ����㣺

��1������26.5%��Na2CO3��Һ80g����ҪNa2CO3���� g��
��2��BaCl2��Һ���������������Ƕ��٣���д��������̣����������0.1%��
(1) 21.2g ��2�֣�
�⣺(2)��ͼ���л�֪����BaCl2��ȫת��Ϊ����ʱ����Na2CO3��Һ������Ϊ40g��
��BaCl2������Ϊx����
BaCl2��Na2CO3��BaCO3����2NaCl
208����106
x������40g��26.5%
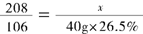
��ã�x��20.8g
��BaCl2��Һ������������������20.8g/150g��x 100%=13.9%
�𣺸�BaCl2��Һ��������������Ϊ13.9%��
�����������������Ҳ���֣�
����������


 �Ǽ�����������ϵ�д�
�Ǽ�����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ��ʾ����֪��BaCl2+Na2CO3=BaCO3��+2NaCl
ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ��ʾ����֪��BaCl2+Na2CO3=BaCO3��+2NaCl �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?������ģ�⣩ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ����ʾ������㣺
��2012?������ģ�⣩ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ����ʾ������㣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2012?�߰���һģ��ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��100g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ��ʾ����֪��BaCl2+Na2CO3=BaCO3��+2NaCl
��2012?�߰���һģ��ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��100g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ��ʾ����֪��BaCl2+Na2CO3=BaCO3��+2NaCl �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��2013?�㶫ģ�⣩ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ��ʾ��
��2013?�㶫ģ�⣩ʵ������һƿδ֪Ũ�ȵ�BaCl2��Һ��ijͬѧȡ��150g����Һ���ձ��У���������μ���������������Ϊ26.5%��Na2CO3��Һ����Ӧ���������ɳ���������������Na2CO3��Һ�����Ĺ�ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com