
| 品名 | 雪碧汽水(清爽柠檬酸味) |
| 配料 | 碳酸水(水,二氧化碳)、果葡萄浆、白砂糖、柠檬酸、香料、苯甲酸钠 |
| 保质期 | 18个月 |
| 注意 | 禁止加热、避免阳光直晒及高温 |
分析 二氧化碳的溶解度随温度的升高而减小,随压强的增大而增大;且能够和水反应生成碳酸,但碳酸很容易分解特别是在加热的条件下,因此加热后若溶液中的石蕊仍为红色,则说明柠檬酸呈酸性.
解答 解:由于二氧化碳气体的溶解度随压强的减小而减小,故答案为:降低;
(1)由于紫色石蕊试液只有遇到酸性溶液才会变红,因此石蕊溶液变红色,说明柠檬酸确实具有酸性,故答案为:紫色石蕊试液只有遇到酸性溶液才会变红;
(2)由于该饮料是碳酸饮料,里面含有碳酸,碳酸也能使紫色石蕊溶液变红,故答案为:汽水中含有碳酸,也能使紫色石蕊试液变红;
(3)由于碳酸在加热条件很容易分解,如果碳酸分解后的溶液仍为红色,就可说明柠檬酸呈酸性,故答案为:加热,溶液为红色.
点评 本题主要考查了酸的某些化学性质及二氧化碳的有关知识,培养学生分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
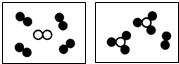 如图A、B、C 3种不同分子的模型分别用○○、●●和表示,如图为3种物质之间发生化学反应前后的状况,则在该反应的化学方程式中,A、B、C这3种物质的化学式前的系数之比为( )
如图A、B、C 3种不同分子的模型分别用○○、●●和表示,如图为3种物质之间发生化学反应前后的状况,则在该反应的化学方程式中,A、B、C这3种物质的化学式前的系数之比为( )| A. | 1:4:3 | B. | 1:3:2 | C. | 1:4:2 | D. | 1:3:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D | 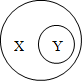 | |
| X | 化合物 | 单质 | 纯净物 | 化学性质 | |
| Y | 氧化物 | 化合物 | 混合物 | 溶解性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
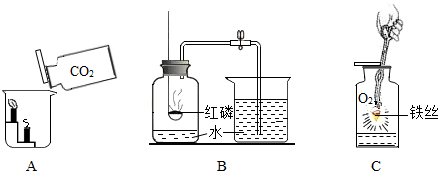
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
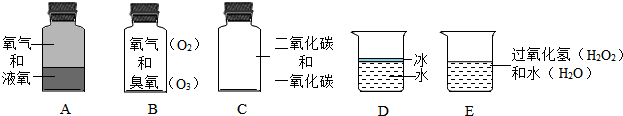
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
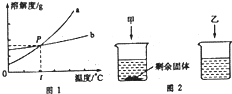
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 245 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用细口瓶盛放固体药品 | B. | 用剩的药品放回原瓶 | ||
| C. | 温度计代替玻璃棒用于搅拌 | D. | 过滤时,倾倒液体用玻璃棒引流 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com