
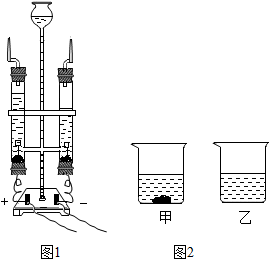
 水是生命之源,水在生活和化学实验中都有广泛的用途.
水是生命之源,水在生活和化学实验中都有广泛的用途.| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
分析 (1)根据明矾溶于水后生成胶状物对杂质的吸附,使杂质沉降解答;蒸馏可以得到纯净水,净化程度最高;吸附可以除去水中的色素和异味;过滤、沉降(静置沉淀)可以除去不溶于水的物质;
(2)电解水时根据“正氧负氢、氢二氧一”进行解答;
(3)
①根据在40℃时,KNO3和KCl溶解度的大小分析;
②根据饱和溶液与不饱和溶液之间的转化关系分析;
③根据欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是:溶液温度不低于t2℃解答;
④根据加水稀释前后溶液中溶质质量不变,利用密度公式和溶质质量分数公式计算可配制成10%的稀硫酸的质量;用配制成的稀硫酸的质量减去浓硫酸的质量便得需要水的质量;
解答 解:
(1)明矾溶于水后生成胶状物对杂质的吸附,使杂质沉降,所以农村常用明矾来净水.
A、吸附沉淀是利用明矾能使水中不溶性固体小颗粒凝聚,而沉降到水底,初步分离;活性炭吸附是除去水中的异味和有色物质.
B、沉降是依靠杂质本身的重力作用,将固体自然沉降到水底,初步分离;
C、过滤可除去水中不溶性固体杂质,所得水还会含有可溶性杂质等;
D、蒸馏,把水通过蒸发、冷凝处理,处理后的水中只含水一种物质,所得水称为蒸馏水为纯净物;因此净化程度最高的方法是蒸馏;
故选D.
(2))电解水时正极产生的是氧气,负极产生的是氢气反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)
①由溶解度可知,在40℃时,KNO3的溶解度是63.9g,KCl的溶解度是40.0g,由乙烧杯的溶质全部溶解了,说明了乙烧杯中的溶质是KNO3;
②A、当升高温度时,烧杯中的剩余固体全部溶解,溶液变为不饱和溶液,溶剂质量不变.故A说法正确;
B.当加入溶剂时,烧杯中的剩余固体全部溶解,溶液变为不饱和溶液,溶液中溶质的质量分数不一定增大.故B说法错误;
C.溶质的质量增加了,溶液质量一定增大.故C说法正确;
D.可采用升温或加水的方法,都可以使烧杯中的剩余固体全部溶解,溶液变为不饱和溶液,故D说法正确;
③欲配制溶质的质量分数为20%的硝酸钾溶液,应满足的温度范围是:溶液温度不低于t2℃;
④设可配制成10%的稀硫酸的质量为x,10mL=10cm3,根据加水稀释前后溶液中溶质质量不变可得:
10%x=1.84g/cm3×10cm3×98%
解得x≈180g;
需要水的质量是:180g-1.84g/cm3×10cm3≈162g;即162ml
答案:
(1)明矾溶于水后生成胶状物对杂质的吸附,使杂质沉降 D
(2)氧气 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(3)
①KNO3
②ACD
③溶液温度不低于t2℃
④要加水162毫升
点评 本题比较全面考查了水的知识,水的在生产和生活中有着广泛应用,应加强有关知识的学习.在解此类题时,首先分析各种操作的净水效果,然后结合具体的情况进行分析.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 化学是以实验为基础的学科,根据实验1、实验2回答下列问题:
化学是以实验为基础的学科,根据实验1、实验2回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碳酸钙可用作补钙剂 | |
| B. | 硫酸铜溶液可以作为自来水的消毒剂 | |
| C. | 食盐可用于调味和腌渍蔬菜、鱼、肉等 | |
| D. | 小苏打是焙制糕点所用的发酵粉的主要成分之一 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题

| A. | 无色溶液B的溶质是硝酸钙 | |
| B. | 原溶液中的杂质一定是氯化钙 | |
| C. | 原溶液中的杂质可能由三种物质组成 | |
| D. | 该实验中涉及的基本反应类型只有一种 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 氯化钾与氯化铵固体 | 熟石灰、研磨 |
| B | 硝酸铵与食盐固体 | 水 |
| C | 氢氧化钠溶液与碳酸钠溶液 | 酚酞溶液 |
| D | 一氧化碳与二氧化碳气体 | 用燃着木条 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com