
���� ����֪������96%������63t�����ɼ��������������������������ɼ��������������������������ݻ�ѧ����ʽ����������������������������20%������ʯ��������Ҳ���Ը�����Ԫ�ص������غ㶨���ɻ�ѧʽ���Լ������Ҫ������ʯ��������
��� �⣺����һ������96%������63t����������Ϊ��63t��96%��
����Ҫ������������Ϊx��
3CO+Fe2O3 $\frac{\underline{\;����\;}}{\;}$2Fe+3CO2
160 112
x 63t��96%
$\frac{160}{112}=\frac{x}{63t��96%}$ ��ã�x=86.4t
��Ҫ����ʯ����Ϊ��$\frac{86.4t}{1-20%}$=108t��
��������������Ԫ�������غ㶨��֪��
X����1-20%����$\frac{2Fe}{F{e}_{2}{O}_{3}}$��l00%=63t��96%��
�ʴ�Ϊ����1��3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2����2��63t��96%����3��$\frac{160}{112}=\frac{x}{63t��96%}$����4��86.4t��
��5��108t������������1-20%����96%��
���� ���������غ㶨�ɵ�˼�봦�����⣻ѧ����㻯����������ijԪ�ص������ķ��������ո��ݻ�ѧ����ʽ����IJ��衢������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������֮��������� | B�� | ��ѧ��Ӧ�Ŀ��� | ||
| C�� | ��ʲô�����·�����Ӧ | D�� | ��Щ���ʲμӷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʯ�Ҹ����������� | B�� | ��θ��ƽ[��Al��OH��3]ҽ��θ����� | ||
| C�� | ����������� | D�� | ���ռ���Һ�������Թ�ǿ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
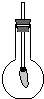 ��ͼ��ʾ���ô��е��ܵ���Ƥ����������������̼�������ƿ�ڣ�����һ��ϵ��һ��С����Ȼ�γ���Ƥ����Ѹ������ƿ�ڵ�������Ũ������������Һ����������ƿ��������������ش�С��������ʲô����Ϊʲô����д����ƿ�ڷ����Ļ�ѧ��Ӧ����ʽ��
��ͼ��ʾ���ô��е��ܵ���Ƥ����������������̼�������ƿ�ڣ�����һ��ϵ��һ��С����Ȼ�γ���Ƥ����Ѹ������ƿ�ڵ�������Ũ������������Һ����������ƿ��������������ش�С��������ʲô����Ϊʲô����д����ƿ�ڷ����Ļ�ѧ��Ӧ����ʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2CO3�TCO2��+H2O | B�� | CO+CuO$\frac{\underline{\;\;��\;\;}}{\;}$Cu+CO2 | ||
| C�� | H2+CuO$\frac{\underline{\;\;��\;\;}}{\;}$Cu+H2O | D�� | S+O2$\frac{\underline{\;��ȼ\;}}{\;}$SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
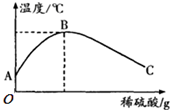 �кͷ�Ӧʱ���ܶ�ͬѧ�������̽����Ȥ��
�кͷ�Ӧʱ���ܶ�ͬѧ�������̽����Ȥ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com