
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
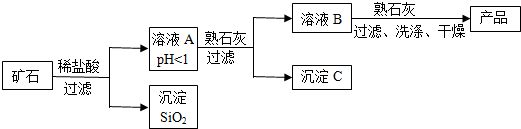
(2)本题考查碱的制备.组成矿石的四种氧化物中仅SiO2不与盐酸反应,其余三种均能反应:
MgO+2HCl═MgCl2+H2O、Fe2O3+6HCl═2FeCl3+3H2O、CuO+2HCl═CuCl2+H2O,溶液A的pH<1,说明反映后溶液呈强酸性,盐酸过量,因此溶液A中的阳离子有Mg2+、Fe3+、Cu2+、H+;要使Mg(OH)2纯度高、损失少,必须把pH控制在氯化铜能完全沉淀、但氯化镁不能沉淀的范围内,即6.7<pH<8.6的范围内;溶液B中一定有氯化镁.
解答 解:(1)工业上用一氧化碳还原赤铁矿石(主要成分为氧化铁)炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.故答案为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)①溶液A中共含有4种阳离子,它们是Mg2+、Fe3+、Cu2+、H+;
故填:4.
②为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可容许的范围为6.7~8.6,即必须把pH控制在氯化铜能完全沉淀、但氯化镁不能沉淀的范围内.
故填:6.7≤pH<8.6;
③当B溶液的pH在6.7~8.6时,铜离子已经完全沉淀,镁离子没有形成沉淀,所以溶液B中一定含有的溶质为氯化镁和反应生成的氯化钙,化学式分别是MgCl2、CaCl2.
故填:MgCl2、CaCl2.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,并有助于提高观察、实验能力.所以,对化学实验不仅要认真观察,还应掌握观察实验现象的方法.


 优加精卷系列答案
优加精卷系列答案科目:初中化学 来源: 题型:填空题
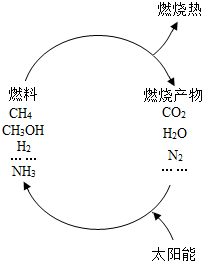 为解决过度使用化石燃料造成的能源危机及环境问题,科学家提出如图的科学构想:
为解决过度使用化石燃料造成的能源危机及环境问题,科学家提出如图的科学构想:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | 氯化氢 | 盐酸 | 氢氧化钙 | 石灰水 | 氯化钠 | 食盐水 |
| 组成元素 | H、Cl | H、Cl、O | Ca、H、O | Ca、H、O | Na、Cl | Na、Cl、H、O |
| 构成粒子 | HCl | HCl、H2O | Ca2+、OH- | Ca2+、OH-、H2O | Na+、Cl- | Na+、Cl-、H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
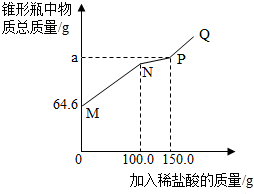 取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸.实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示.(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑)下列说法正确的是( )
取14.6g变质的氢氧化钠固体样品(不含水)于锥形瓶中,加入50.0g水,充分溶解,再向锥形瓶中滴加的溶质质量分数为7.3%的稀盐酸.实验测得加入稀盐酸的质量与锥形瓶中物质的总质量关系如图所示.(资料酸钠与稀盐酸反应分两步进行:Na2CO3+HCl═NaHCO3+NaCl,NaHCO3+HCl═NaCl+H2O+CO2↑)下列说法正确的是( )| A. | N点的溶液表示氢氧化钠被恰好完全反应 | |
| B. | PQ段(不含P点)溶液的pH<7 | |
| C. | NP段表示产生气体的过程,a的值为210.2 | |
| D. | 该固体样品中氢氧化钠的质量为8.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中一定有Ag,没有Cu和Zn | |
| B. | 滤渣中一定有Ag和Zn,可能有Cu | |
| C. | 滤液中一定有Zn(NO3)2、Cu(NO3)2,可能有AgNO3 | |
| D. | 滤液中一定有Zn(NO3)2、Cu(NO3)2、AgNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4 NH4Cl ZnCl2 | B. | NaOH NaCl NaNO3 | ||
| C. | CuSO4 NaCl KNO3 | D. | K2SO4 AgNO3 NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com