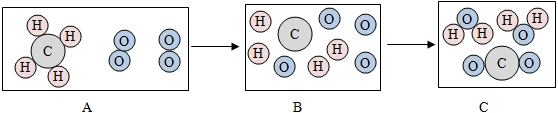
某同学在敞口容器中做了两个实验:一是氧化汞(HgO)受热分解生成汞和氧气;二是铝粉在氧气中燃烧生成固体氧化铝.他准确称量了反应前后容器及所盛物质的质量,发现反应前后质量都发生了变化.请填空:
(1)铝粉燃烧生成氧化铝的质量比参加反应铝粉的质量______(选填“大”、“小”或“不变”),原因是______.
(2)你认为这两个反应是否遵循质量守恒定律?______(选填“是”或“否”),若要用上述两个实验验证质量守恒定律,则要做的改进是______.
(3)请写出氧化汞受热分解的化学方程式:______.
解:(1)根据质量守恒定律,铝粉在氧气中燃烧生成氧化铝,氧化铝的质量应等于参加反应的铝的质量加上反应的氧气的质量,因此生成氧化铝的质量比参加反应铝粉的质量大.
故答案为:大;
(2)化学变化都遵守质量守恒定律,有气体参加反应的实验应在密闭容器内进行反应.
故答案为:是;在密闭容器内进行反应;
(3)氧化汞在加热的条件下生成汞和氧气,配平即可.
故答案为:2HgO

2Hg+O
2↑.
分析:(1)根据质量守恒定律分析,质量守恒定律的内容是:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.铝粉在氧气中燃烧生成氧化铝,氧化铝的质量大于铝的质量;
(2)化学变化都遵守质量守恒定律;有气体参加反应的实验应在密闭容器内进行;
(3)氧化汞在加热的条件下生成汞和氧气,配平即可.
点评:本考点是有关质量守恒定律的实验探究和化学方程式的书写,有关质量守恒定律的考题在中考中经常出现,要抓住要点:五个一定不变,一个一定变.还要注意药品的选择和装置的选择、反应容器的严密性等.

 2Hg+O2↑.
2Hg+O2↑.

 一本好题口算题卡系列答案
一本好题口算题卡系列答案 质量守恒定律的定量研究对化学科学发展具有重大意义.
质量守恒定律的定量研究对化学科学发展具有重大意义. ”和“
”和“ ”分别表示两种不同的原子:
”分别表示两种不同的原子: ”聚集成的物质
”聚集成的物质