
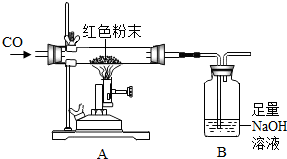
 某化学兴趣小组.对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组.对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和的总质量为48.3 | 玻璃管和固体的总质量为47.1 |
| Ⅱ 组 | 洗气瓶和瓶所盛的总质量为258.6 | 洗气瓶和瓶所盛的总质量为261.9 |
| 48 |
| 160 |
| 4g |
| 5g |
| 48 |
| 160 |
| 4g |
| 5g |
| 106 |
| 44 |
| 50g?x |
| 2.2g |
| 73 |
| 44 |
| y |
| 2.2g |
| 40 |
| 36.5 |
| z |
| 0.73g |


科目:初中化学 来源: 题型:
| 实验方法 | 实验现象 | 结论 |
| NaOH溶液浓度过大 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
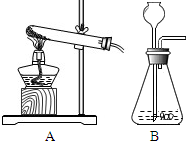 如图所示是常见的气体发生装置,请回答问题:
如图所示是常见的气体发生装置,请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com