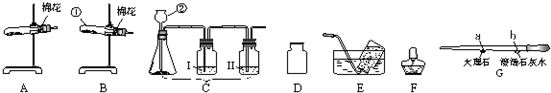
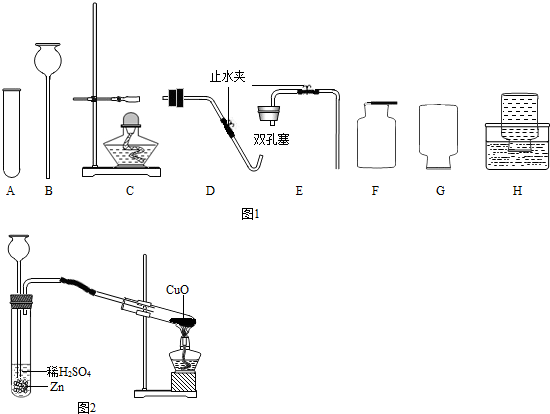
解:(1)仪器G是集气瓶;
(2)检查装置气密性的方法是:将导管的一端放入水中,用手紧握试管一会儿,若导管口有连续的气泡冒出,手松开后水倒吸,则气密性良好;
(3)实验室制取二氧化碳用大理石和稀盐酸,不需加热,可用A作为反应容器,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,可用F或I,选择E双孔塞,长颈漏斗;连接玻璃棒和胶皮管的方法是把玻璃管口用水润湿,然后稍微用力,即可把玻璃管插入橡皮管中.二者反应生成氯化钙、水和二氧化碳,方程式是:CaCO
3+2HCl=CaCl
2+CO
2↑+H
2O;二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠可用于造纸、玻璃、印染、洗涤剂,碳酸钠和盐酸反应生成氯化钠,氯化钠有咸味,可作为调味品,还可用来配制生理盐水;
(4)甲烷的密度比空气小,故应从短管进气,将空气挤压到集气瓶底部排出,甲烷和氧气在点燃的条件下反应生成二氧化碳和水,方程式是CH
4+2O
2
CO
2+2H
2O;
故答案为:(1)集气瓶;
(2)将导管的一端放入水中,用手紧握试管一会儿,若导管口有连续的气泡冒出,手松开后水倒吸,则气密性良好;
(3)ABEF或者ABEI; 用水润湿; CaCO
3+2HCl═CaCl
2+H
2O+CO
2↑; 碳酸钠:作洗涤剂;氯化钠:作调味品(合理均可);
(4)b; CH
4+2O
2
CO
2+2H
2O.
分析:(1)据常用仪器回答;
(2)据检查气密性的方法回答;
(3)据反应物状态和反应条件选择发生装置所用仪器,据气体的密度和溶解性选择收集装置;连接玻璃棒和胶皮管的方法是把玻璃管口用水润湿,然后稍微用力,即可把玻璃管插入橡皮管中.据反应原理书写方程式;二氧化碳与氢氧化钠反应生成碳酸钠,碳酸钠和盐酸反应生成氯化钠,并结合碳酸钠和氯化钠的用途回答;
(4)甲烷的密度比空气小,故应从短管进气,并结合甲烷燃烧反应原理书写方程式.
点评:本题考查知识较为全面,提醒同学们要注意基础知识的积累,并能结合具体情景分析解答相关问题,能较好培养学生分析解决问题的能力.


 CO2+2H2O;
CO2+2H2O; CO2+2H2O.
CO2+2H2O.