碳元素形成的单质和化合物的种类是元素中最多的.我们已经学习了①金刚石、②石墨、③CO、④CO2、⑤CaCO3等,还有许多有机物.据美国《science》期刊报道,近几年又陆续发现了⑥C540、⑦C3O2、⑧C4O3、⑨C5O2等物质.根据上述材料回答以下问题:
(1)其中属于单质的是 (填编号).
(2)某种碳的氧化物含碳量为50%,写出C和CO2在高温下转化为该氧化物的化学方程式 .
(3)写出C3O2完全转化为CO2和另一种碳的氧化物的化学方程式(不必注明反应条件) .
(4)汽车尾气中含有CO和氮的氧化物等有毒气体.现已发明一种装有特殊催化剂的装置,使氮的氧化物(用NOX表示)与CO相互反应生成N2和CO2.其化学方程式为: .
【答案】
分析:(1)由同种元素构成的纯净物为单质,由不同种元素构成的纯净物为化合物;
(2)由这种氧化物中碳元素的含量为50%,可求出氧化物的化学式,然后由反应物和生成物,根据质量守恒定律书写化学方程式;
(3)根据化学反应前后原子的个数不变书写化学方程式.
解答:解:(1)由单质和化合物的定义,可知:①金刚石、②石墨、⑥C
540都是由碳元素构成的纯净物,为单质,③CO、
④CO
2、⑤CaCO
3、⑦C
3O
2、⑧C
4O
3、⑨C
5O
2都是由不同种元素构成的纯净物,为化合物;
(2)设这种碳的氧化物的化学式为C
xO
y,由碳含量为50%,可知

×100%=50%,则
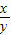
=

,该氧化物的化学式为C
4O
3,C和CO
2在高温下转化为该氧化物的化学方程式为:5C+3CO
2
2C
4O
3;
(3)完全转化为CO
2和另一种碳的氧化物,根据质量守恒定律,2个C
3O
2分子中含有6个碳原子、4个氧原子,一个CO
2分子含有1个碳原子、2个氧原子,则另一种氧化物中应含有5个碳原子、2个氧原子,化学式为C
5O
2;C
3O
2完全转化为CO
2和C
5O
2的化学方程式:2C
3O
2═CO
2+C
5O
2;
(4)氮的氧化物(用NO
X表示)与CO相互反应,生成N
2和CO
2.其化学方程式为:2NO
x+2xCO

N
2+2xCO
2.
故答案为:
(1)①②⑥;
(2)5C+3CO
2
2C
4O
3;
(3)2C
3O
2
CO
2+C
5O
2;
(4)2NO
x+2xCO═N
2+2xCO
2.
点评:熟记单质和化合物的概念,写方程式注意反应物、生成物、反应条件,利用质量守恒定律配平.

 ×100%=50%,则
×100%=50%,则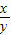 =
= ,该氧化物的化学式为C4O3,C和CO2在高温下转化为该氧化物的化学方程式为:5C+3CO2
,该氧化物的化学式为C4O3,C和CO2在高温下转化为该氧化物的化学方程式为:5C+3CO2 2C4O3;
2C4O3; N2+2xCO2.
N2+2xCO2. 2C4O3;
2C4O3; CO2+C5O2;
CO2+C5O2;

 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案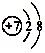 可知,氮原子最外层电子数目为
可知,氮原子最外层电子数目为