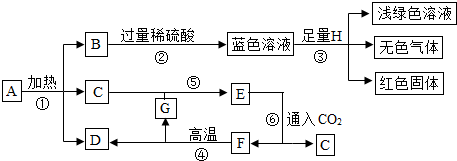
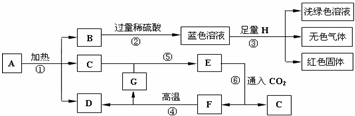
解:由于F是常用的建筑材料,所以F为碳酸钙,碳酸钙高温生成氧化钙、二氧化碳,即GD应该为二氧化碳和氧化钙,由于E通入二氧化碳生成F碳酸钙,推出E是氢氧化钙,C是水,C和G反应生成氢氧化钙,所以G是氧化钙,D是二氧化碳;B与过量稀硫酸反应,得到蓝色溶液,由于蓝色溶液是铜离子的溶液,所以蓝色溶液是硫酸铜溶液,里面还有过量的稀硫酸;H是单质并且与蓝色溶液反应,生成浅绿色溶液、无色气体、红色固体,所以H是铁,浅绿色溶液是硫酸亚铁、无色气体是氢气、红色固体是铜;
由于B与过量硫酸反应生成硫酸铜,且B是一个分解反应得到的三种物质之一,即一定为碱式碳酸铜分解的结果,所以B是氧化铜;因为A加热生成氧化铜、水、二氧化碳,所以A是碱式碳酸铜.
综上所述:
A 为Cu
2(OH)
2CO
3; B 为CuO; C 为H
2O; D 为CO
2;E 为Ca(OH)
2;F 为CaCO
3;G 为CaO; H 为Fe;
(1)由分析知A是Cu
2(OH)
2CO
3;蓝色溶液中含有的溶质是CuSO
4和H
2SO
4;
(2)由分析知各步的反应方程式为①Cu
2(OH)
2CO
3
2CuO+H
2O+CO
2↑;②H
2SO
4+CuO═CuSO
4+H
2O;③Fe+CuSO
4=Cu+FeSO
4 Fe+H
2SO
4=FeSO
4+H
2;④CaCO
3
CaO+CO
2↑;⑤CaO+H
2O=Ca(OH)
2;⑥CO
2+Ca(OH)
2═CaCO
3↓+H
2O;置换反应是单质与化合物生成单质与化合物的反应,所以③属于置换反应;
(3)“石灰吟”中诗句“粉身碎骨浑不怕”包含的化学变化用化学方程式表示为:CaO+H
2O=Ca(OH)
2;
故答案为:(1)Cu
2(OH)
2CO
3;CuSO
4;H
2SO
4;(2)Fe+CuSO
4=Cu+FeSO
4; Fe+H
2SO
4=FeSO
4+H
2;(3)CaO+H
2O=Ca(OH)
2;
分析:首先,依据物质的特性,找出突破口,F是常用的建筑材料,所以为碳酸钙,再根据蓝色溶液是铜离子的溶液,浅绿色溶液是亚铁离子溶液,红色固体通常是铜,再根据物质间的反应进一步进行推断.
点评:解物质的推断题时,先根据物质的特性和用途等找出解题的突破口,再根据物质间的反应逐一分析.

 2CuO+H2O+CO2↑;②H2SO4+CuO═CuSO4+H2O;③Fe+CuSO4=Cu+FeSO4 Fe+H2SO4=FeSO4+H2;④CaCO3
2CuO+H2O+CO2↑;②H2SO4+CuO═CuSO4+H2O;③Fe+CuSO4=Cu+FeSO4 Fe+H2SO4=FeSO4+H2;④CaCO3 CaO+CO2↑;⑤CaO+H2O=Ca(OH)2;⑥CO2+Ca(OH)2═CaCO3↓+H2O;置换反应是单质与化合物生成单质与化合物的反应,所以③属于置换反应;
CaO+CO2↑;⑤CaO+H2O=Ca(OH)2;⑥CO2+Ca(OH)2═CaCO3↓+H2O;置换反应是单质与化合物生成单质与化合物的反应,所以③属于置换反应;

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案