
【题目】下图是实验室制取气体的常用装置。请回答下列问题。
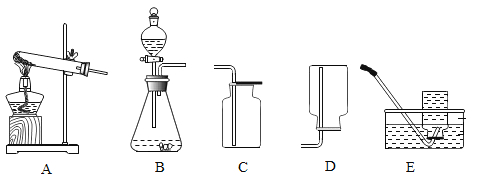
(1)实验室制取气体时,组装好仪器后,应先_____,再添加药品。
(2)实验室选择气体发生装置时,应考虑的因素是_____。
(3)实验室可用上图中的装置来制备和收集一些常见的气体, 请用化学方程式和上图中字母序号填写下表空白。
制取的气体 | 反应原理(用化学方程式表示) | 发生装置 | 收集装置 |
O2 | _____ | A | _____ |
CO2 | _____ | B | D |
(4)通常状况下,甲烷是一种无色无味气体,难溶于水,密度比空气小。实验室常用醋酸钠和碱石灰两种固体混合加热制得,制取并收集甲烷可选用的装置是_____。
(5)图F是某同学利用报废试管设计的制取二氧化碳的发生装置, 该设计除了废物利用的优点外,请另写一个优点: _____。
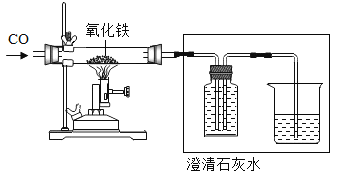
(6)下图是一氧化碳与氧化铁的反应装置中,虚线方框内装置的作用是_____。
【答案】检查装置气密性 反应物的状态和反应条件 2KClO3![]() 2KCl+3O2↑ D或E
2KCl+3O2↑ D或E ![]() AC或AE 可以控制反应的发生或停止 检验并除去反应生成的二氧化碳,收集尾气中的CO
AC或AE 可以控制反应的发生或停止 检验并除去反应生成的二氧化碳,收集尾气中的CO
【解析】
(1)制取气体时,组装好仪器后,应先检查装置的气密性,再添加药品。
(2)实验室选择气体发生装置时,应考虑的因素是反应物的状态和反应的条件;如果是用固体或固体混合物在加热的条件下反应制取气体,那么就要选择 “固体加热型”的装置;如果是用固体和液体混合物在常温的条件下反应制取气体,那么就要选择 “固液常温型”的装置。
(3)装置A适用于固体加热制取气体,因为试管口处,没有棉花团,所以是加热氯酸钾与二氧化锰的混合物制取氧气,同时生成氯化钾,反应方程式为:2KClO3![]() 2KCl+3O2↑氧气的密度比空气大,不易溶于水,可用向上排空气法或排水法来收集,装置为D或E;
2KCl+3O2↑氧气的密度比空气大,不易溶于水,可用向上排空气法或排水法来收集,装置为D或E;
实验室中常用大理石或石灰石(主要成分是碳酸钙)与稀盐酸反应来制取二氧化碳,同时生成氯化钙和水,反应方程式为:![]() ,该反应属于固液常温型,选择装置B来制取;二氧化碳的密度比空气大,能溶于水,可用向上排空气法收集;
,该反应属于固液常温型,选择装置B来制取;二氧化碳的密度比空气大,能溶于水,可用向上排空气法收集;
(4)通常状况下,甲烷是一种无色无味气体、难溶于水、密度比空气小,故收集甲烷可以使用排水法或是向下排空气法,实验室常用醋酸钠和碱石灰两种固体混合加热制得,是固体加热型反应,故制取并收集甲烷可选用的装置是AC或AE;
(5)图F是某同学利用报废试管设计的制取二氧化碳的发生装置, 该设计除了废物利用的优点外,请另写一个优点:可以控制反应的发生或停止。
(6)一氧化碳与氧化铁在高温的条件下生成铁和二氧化碳,二氧化碳能使澄清石灰水变浑浊,故澄清石灰水能检验并除去反应生成的二氧化碳,一氧化碳有毒且难溶于水,C虚线方框内装置,则还起到的作用是用排水法收集一氧化碳气体;故虚线方框内装置的作用是:检验并除去反应生成的二氧化碳,收集尾气中的CO。


科目:初中化学 来源: 题型:
【题目】A~F均为初中化学常见的物质,它们之间的关系如下图所示(“→”表示转化关系,涉及反应为初中常见反应),其中 A 俗名为生石灰,C为常见的溶剂,C 与 E 元素组成相同。请回答下列问题:
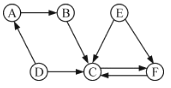
(1)F 的化学式为______。
(2)B 在农业上的用途是______(写一种)。
(3)转化中没有涉及的基本反应类型是______ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)有关资料介绍,制取氧气有多种方法,其中氧化铜与氯酸钾混合加热,也能很快产生氧气。现将2.5g氧化铜与24.5g氯酸钾的混合物充分加热,残余固体经冷却、称量、质量为17.4g。然后将固体溶于65.1 g水中,充分搅拌,过滤得到滤液和黑色的滤渣。滤渣又经过洗涤、烘干、称量,质量为2.5g。(不考虑过程中物质的损失,计算结果保留一位小数)
(1)该反应中氧化铜起 作用。
(2)生成的氧气为 克。
(3)所得滤液中溶质是 ,其质量分数为 。
(4)向所得滤液中加入质量分数为16%的AgNO3溶液恰好完全反应,需AgNO3溶液的质量为多少克?(列出必要的计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室中常见的气体制备、干燥、净化、收集和性质实验的部分仪器,甲、乙两组同学欲用它们完成各自的探究实验。
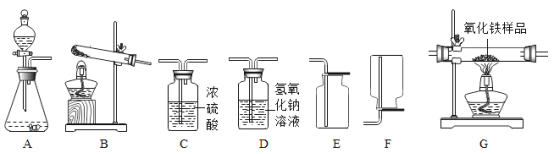
(1)甲组同学以锌粒和稀盐酸为原料制取氢气,因盐酸挥发出少量的氯化氢气体,导致制取的气体不纯,现欲制备并收集一瓶干燥、纯净的氢气,回答下列问题:
①所选仪器的连接顺序为_______。
②反应装置中生成氢气的化学方程式_______。
③锌与稀盐酸混合后,随着反应的进行,盐酸溶液的pH将______(填“增大”“减小”“不变”“无法判断”之一)
(2)乙组同学欲用水煤气(主要成分为一氧化碳、氢气,含有少量水蒸气)来测定氧化铁样品中Fe2O3的纯度,设计的仪器连接顺序为:水煤气→C1→G→C2→D→C3. (已知:氧化铁样品中的杂质不反应;.![]() ;
; 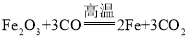 ;其中C1、C2、C3为3个浓硫酸洗气瓶)
;其中C1、C2、C3为3个浓硫酸洗气瓶)
①写出G中的一项实验现象______。
②该同学通过测量反应前后G装置质量的变化,来计算样品中Fe2O3的纯度,若无装置C1,则计算结果会____(填“偏大”“偏小”、“基本一致”之一)。
③实验中该小组学生取用了25g氧化铁样品,经实验测定装置C2增加了2.7g,D装置增加了6.6g,则氧化铁样品的纯度为______。
④从环境保护的角度考虑,该套实验装置存在不足,写出具体改进措施________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)从铁、二氧化碳、高锰酸钾、硫酸铜溶液、水、氢氧化钠溶液、稀盐酸中选择适当物质,分别写出符合下列要求的化学方程式,每种物质只能用一次。
①化合反应:________;
②分解反应:______;
③置换反应:________;
(2)在一个密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下表所示:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 5 | 2 | 20 | 22 |
反应后质量/g | 待测 | 11 | 28 | 5 |
该反应所属的基本反应类型是_______。
(3)下图所示是某化学反应前后的微观模拟图,该化学反应中,参加反应的“![]() ”和“
”和“![]() ”与反应后生成的“
”与反应后生成的“![]() ”各粒子间的个数比为______。
”各粒子间的个数比为______。
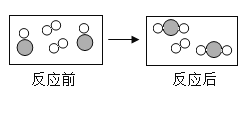
(4)下图所示是某密闭容器中物质变化过程的微观示意图(其中“![]() ”代表氧原子,“
”代表氧原子,“![]() ”代表硫原子),请回答下列问题:
”代表硫原子),请回答下列问题:
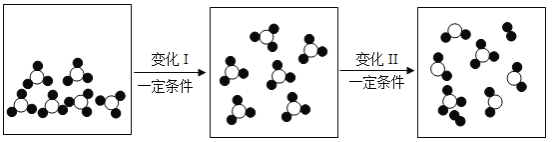
①变化I中的“一定条件”可能是_____(写出一项即可);
②变化Ⅱ发生的是______(填序号)。
A 化合反应 B 分解反应 C 置换反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学课外兴趣小组欲配制80g质量分数为12%的氢氧化钠溶液来制作“叶脉书签”。
(1)需要氢氧化钠固体的质量为__________g。
(2)称量时,氢氧化钠固体应放在__________(填“滤纸”或“烧杯”)中。
(3)下列说法或操作正确的是__________(填字母序号)。
A配制该溶液时所需的玻璃仪器中不包括玻璃棒
B用量程为100mL的量筒量取所需要的水
C将称量好的固体倒入装有水的量筒中溶解
(4)在量取水的体积时,若采用仰视的方法读数,则所配制的氢氧化钠溶液中溶质的质量分数将__________(填“偏大”或“偏小”)。
(5)某同学用蒸馏水润湿了的pH试纸来测定配制好的溶液的pH值时,他测得的结果会__________(填“偏大”、偏小”或“不变”)。
(6)该兴趣小组的同学提出还可以用配制好的氢氧化钠溶液和稀盐酸进行中和反应实验,具体操作如下图:
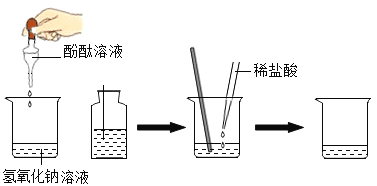
在烧杯中加入10mL的氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液呈__________色。接着加入一定量的稀盐酸,用玻璃棒搅拌后发现溶液为无色,此时__________(填“能”或“不能”)得出两者恰好中和的结论。以下操作及实验现象能证明加入的盐酸为过量的是__________(填字母序号)。
A加入少量铁粉,无明显现象
B滴加紫色石蕊溶液,搅拌后溶液变蓝
C加入碳酸钠溶液,产生气泡
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组用如图装置探究分子的运动。
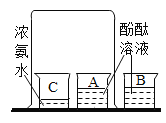
(1)选用药品时利用了浓氨水的以下性质,其中属于浓氨水化学性质的是________;
A 浓氨水有很强的挥发性 B 浓氨水能使酚酞溶液变红色
(2)将酚酞溶液分别倒入A、B两个小烧杯中,另取一个小烧杯C,加入约5 mL浓氨水。用一个大烧杯罩住A、C两个小烧杯。
(发现问题)烧杯A中的酚酞溶液是怎么变成红色的?
(假设一)空气中有一种物质的粒子(分子),不断运动进入A烧杯中,使酚酞溶液变红色。
(假设二)______________________________________________。
(分析)试验中B烧杯内的酚酞溶液_________,说明假设一不正确,假设二是正确的。
(3)B烧杯在实验中是不可缺少的,它体现了一种科学实验的方法,这种方法是________。
(4)请你通过日常生活中实例或设计一个实验来证明分子在不断运动。_____________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明在协助老师清理实验室时,发现有一瓶碳酸钠和氯化钠组成的混合液。他想测定该溶液中碳酸钠和氯化钠的质量分数,为此设计并进行了如下实验。
【实验1】取该混合液50 g ,向其中逐滴加入稀盐酸,当加入稀盐酸的质量为20 g、40 g、60 g 时,生成气体的质量见下表(气体的溶解度忽略不计)。
【实验2】另取该溶液50 g ,加入一定量稀盐酸充分反应后,测得溶液的pH=7,然后再加入硝酸银溶液,测得实验数据见右图。

试分析计算:
(1)【实验1】中,第二组数据 m 为 g。
(2)混合液中碳酸钠的质量分数是多少?
(3)混合液中氯化钠的质量分数是多少?(计算结果精确至0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com