
【题目】在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)在氧气、铁和氯化钠三种物质中,保持氧气化学性质的最小粒子是___________;由离子构成的物质是__________________。
(2)某化学反应的微观示意图如下:
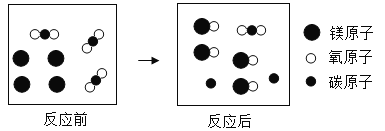
①反应涉及到的物质中,![]() 是由___________(填“分子”、“原子”或“离子”)构或的单质,有____________种氧化物.
是由___________(填“分子”、“原子”或“离子”)构或的单质,有____________种氧化物.
②参加反应的![]() 和
和![]() 的微粒个数比是____________(写出最简整数比)
的微粒个数比是____________(写出最简整数比)
③反应生成的单质和化合物的质量比是_______________
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】硫酸亚铁铵是一种重要的化工原料,用途十分广泛。硫酸亚铁铵俗称摩尔盐,下图为制取摩尔盐过程的示意图。

请回答下列问题:
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍。碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH_____7(填“>”、“<”或“=”)。
(2)步骤②中,过滤操作,需要的玻璃仪器有烧杯、玻璃棒、_____,能用加热蒸发冷却的方法析出,说明摩尔盐的溶解度_____;
(3)废铁屑的主要成分是铁,同时含有少量氧化铁。请写出①中反应的化学方程式_____(写出其中一个化学反应方程式)
(4)步骤②所得滤液中一定含有的溶质是_____;
(5)能用酒精洗涤的原因_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“宏观一微观一符号”三重表征是化学独特的表示物质及其变化的方式。
(1)请结合如图1所示反应的微观图回答下列问题:
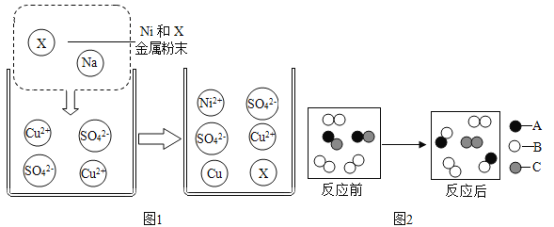
①图1反应中实际参与化学反应的粒子是_____。
②观察到的实验现象是_____。
③三种金属的活动性由强到弱的顺序是_____。
(2)如图2所示化学反应的生成物中有_____种单质。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
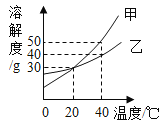
A. 40℃时,等质量的甲、乙形成饱和溶液质量:甲>乙
B. 将等质量的甲、乙两种溶液从40℃降温至20℃时析出的晶体:甲>乙
C. 20℃时,等质量的甲、乙饱和溶液中溶质的质量分数一定相等
D. 40℃时,将30g的乙物质加入到50g水中可形成乙的不饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】利用如图装置进行下列实验(烧杯中放着一支燃着的蜡烛),打开K。
(1)广口瓶中发生反应的化学方程式是________。
(2)观察到蜡烛________,说明影响燃烧剧烈程度因素之一是_________。
【答案】 2H2O2 ![]() 2H2O + O2↑ 燃烧更旺 氧气浓度
2H2O + O2↑ 燃烧更旺 氧气浓度
【解析】本题考查了用过氧化氢制氧气和探究影响燃烧剧烈程度因素。
(1)广口瓶中发生反应是常温下制氧气,应用过氧化氢在二氧化锰催化作用下分解生成水和氧气,化学方程式是2H2O2 ![]() 2H2O + O2↑;
2H2O + O2↑;
(2)观察到蜡烛燃烧更旺;蜡烛在氧气比在空气燃烧更旺,氧气中氧气浓度高于空气中的氧气浓度,说明影响燃烧剧烈程度因素之一是氧气浓度。
【题型】简答题
【结束】
25
【题目】用下图所示实验装置测定空气中氧气含量。
(1)左图中,发生反应的化学方程式为________。
(2)右图中,CD段气压变化的原因是________。
(3)实验前广口瓶内空气体积为V,烧杯中水的体积为V1;实验后烧杯中剩余水的体积为V2。计算空气中氧气体积分数的表达式为_______(用V、V1、V2表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,对于该图象的理解,有下列说法,其中正确的是( )
①B表示铁和稀硫酸的反应曲线
②反应结束后铁一定有剩余锌可能有剩余
③反应结束后消耗的稀硫酸质量相等
④反应结束后生成氢气的质量相等
⑤反应结束后所得溶液质量相等。
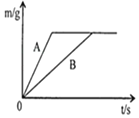
A. ①③④B. ①③⑤C. ①②③④D. ②④⑤
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
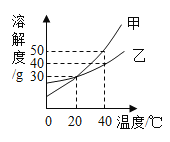
A. 20℃时,甲、乙两种固体物质的溶解度都是30
B. 40℃时,甲的饱和溶液中溶质质量分数为50%
C. 将130g 20℃时甲的饱和溶液升温到40℃,最多还能溶解甲物质20g
D. 40℃时,将50g乙物质全部溶于水中,恰好能得到150g乙的饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组在一次实验活动中发现镁、钠都能在纯净的二氧化碳气体中燃烧,反应后冷却,瓶底除了有黑色颗粒,瓶壁上还都附着白色物质。经检验,黑色颗粒是碳。他们对镁、钠在二氧化碳气体中燃烧后生成的白色物质分别进行了如下探究:
(探究问题一)镁在纯净的二氧化碳中燃烧生成的白色物质是什么?
同学们首先排除了是Mg(OH)2的可能性,理由是_____。
(做出猜想)白色固体可能是①MgO、②MgCO3、③_____。
(进行实验)取少量白色固体,加入足量的稀盐酸,观察到_____现象,猜想①正确。
(实验结论)镁在二氧化碳中燃烧的化学方程式是_____。
(探究问题二)钠在纯净的二氧化碳中燃烧生成的白色物质是什么?
(查阅资料)信息1:钠能与冷水发生剧烈反应。
信息2:Na2O+H2O=2NaOH
(实验设计)甲组方案:
实验步骤 | 实验现象 | 结论 |
取少量白色物质于试管中,加水溶解,加入足量Ba(OH)2溶液 | _____ | 白色物质中有Na2CO3 |
静置后,向上层清液滴加酚酞试液 | 溶液变红 | 白色物质中有Na2O |
甲组结论:白色固体为Na2O和Na2CO3的混合物
乙组方案:
取5.3克白色固体样品进行下列操作:
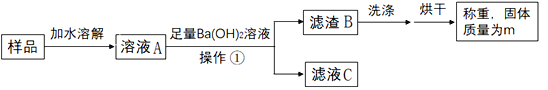
(1)操作①是_____。
(2)Ba(OH)2溶液必须足量的目的是_____。
该组同学测得m=9.85克,结合样品质量进行分析,最终得出结论:白色固体为Na2CO3。
(实验反思)
(1)为何甲、乙两组所得结论不相符,某同学分析后指出甲组方案不科学,应该将甲组方案中的Ba(OH)2溶液改为_____溶液才合理。
(2)钠在二氧化碳中燃烧的化学方程式为_____。
(拓展应用)
实验室里钠等金属因燃烧引发火灾时,可以选择的灭火方式有_____。
A 用水浇灭 B 用液态二氧化碳灭火器 C 撒沙土盖灭
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校兴趣小组的同学为了测定某石灰石中碳酸钙的质量分数,他们取该石灰石样品10g加入烧杯中,再把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的杂质既不溶于水,也不与稀盐酸反应):
实验次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 |
加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
剩余固体的质量/g | 6 | m | 1.2 | 1.2 |
分析表中数据,完成下列问题:
(1)表中m的数值为___;
(2)计算稀盐酸的溶质质量分数____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com