
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗涤剂洗油污,是利用它能乳化油污的性质 | |
| B. | 氮气用来保护粮食,是利用氮气常温下化学性质稳定 | |
| C. | 稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光 | |
| D. | 氧气用于火箭发射,是利用氧气的可燃性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
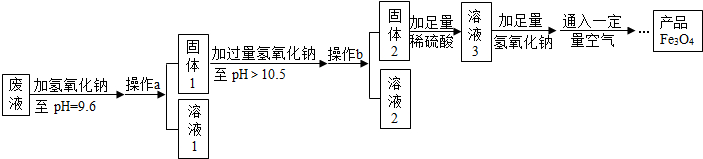
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2、O2、N2 | B. | HCl、H2SO4、Na2SO4 | ||
| C. | NaOH、KOH、NH3•H2O | D. | NaCl、Na2CO3、NH4Cl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com