
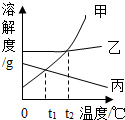
 如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是( )| A、t1℃时,把甲的不饱和溶液变为饱和溶液,溶剂质量一定不变 |
| B、t2℃时,甲、乙两种物质饱和溶液的溶质质量分数一定相等 |
| C、将t1℃时的甲、乙、丙三种物质的饱和溶液升温到t2℃,三种溶液的溶质质量分数大小关系是:甲=乙>丙 |
| D、若甲中混有少量乙,可采用蒸发结晶的方法提纯甲 |
| 溶解度 |
| 溶解度+100g |


科目:初中化学 来源: 题型:
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 31.6 | O.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A、物质C一定是化合物,物质D可能是单质 |
| B、反应后密闭容器中A的质量为19.7g |
| C、反应过程中,物质B与物质D变化的质量比为87:36 |
| D、该反应为化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、碳、氢、氧元素的质量比为6:1:8 |
| B、.醋酸分子中含有氧分子 |
| C、.醋酸不是氧化物 |
| D、.醋酸分子中碳、氢、氧原子个数比为1:2:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、小红提出:呼出的气体水蒸气含量比空气中水蒸气含量少 |
| B、取用石灰水时,实验设计中未说明用量,小东取了1.5ml |
| C、亮亮认为在人呼出的气体中氧气比空气中多 |
| D、小红认为人呼出的气体只有二氧化碳存在 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、铕元素的原子核内的质子数为63 |
| B、铕元素的原子核内的中子数为63 |
| C、铕元素的原子核外电子数为89 |
| D、铕元素的原子的质量为152 |
查看答案和解析>>
科目:初中化学 来源: 题型:
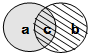 图中的a圆表示化合反应,b圆表示氧化反应,c是它们相交的区域,下列化学反应中,属于c的是( )
图中的a圆表示化合反应,b圆表示氧化反应,c是它们相交的区域,下列化学反应中,属于c的是( )A、CaCO3
| ||||
B、C3H8+5O2
| ||||
C、S+O2
| ||||
D、H2+Cl2
|
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物 质 | 样 品 | 消耗稀盐酸质量 | 反应后溶液质量 |
| 质量(g) | 9 | 75.4 | 80 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com